题目内容
【题目】电化学降解法可用于治理水中硝酸盐的污染,其原理如图。下列说法不正确的是( )
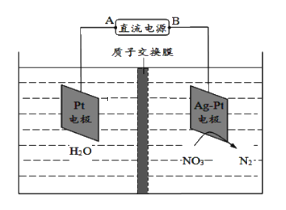
A.A为电源正极
B.在Pt电极上发生氧化反应
C.阴极的电极反应式为:2NO3- + 6H2O + 10e- = N2 + 12OH-
D.若电路转移10mol e-,质子交换膜右侧溶液质量减少18g
【答案】C
【解析】
根据装置图,右边NO3-→N2,N的化合价降低,根据电解原理,右边电极为阴极,左边为阳极,装置中有质子交换膜,说明溶液为酸性,据此分析。
A.根据装置图,右边电极NO3-→N2,N的化合价由+5价→0价,化合价降低,根据电解原理,右边电极为阴极,左边电极为阳极,即A为正极,B为负极,故A正确;
B.根据选项A的分析,Pt电极为阳极,即该电极上发生氧化反应,故B正确;
C.交换膜为质子交换膜,只允许H+通过,说明电解质溶液显酸性,其电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,故C错误;
D.阴极反应式为2NO3-+10e-+12H+=N2↑+6H2O,电路中转移10mol e-,生成1mol N2,即产生28g H2,同时从左边向右边移动10mol H+,即右边溶液质量减少(28g-10g)=18g,故D正确;
答案:C。

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:
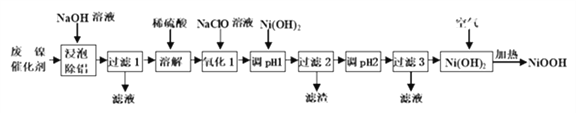
回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;
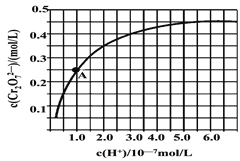
(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。