题目内容
19.下列说法正确的是( )| A. | 在101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ热量,H2的燃烧热为-285.8kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度 | |
| C. | 在101k Pa时,1mol C与适量O2 反应生成1mol CO时,放出110.5kJ热量,则C的燃烧热为110.5kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l),△H=-57.31 kJ•mol-1.若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
分析 燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
A.氢气的燃烧热是指:1mol氢气完全燃烧生成液态水放出的热量;
B.中和热测定时,必须测定起始温度和反应最高温度;
C.碳生成稳定氧化物为二氧化碳;
D.浓硫酸稀释放出大量的热.
解答 解:A.在101kPa时,1mol H2完全燃烧生成液态水,放出285.8kJ热量,符合燃烧热的定义,所以H2的燃烧热为-285.8kJ•mol-1,故A正确;
B.中和热测定时,虽然必须测定起始温度和反应后温度,即反应开始前酸和碱的温度,反应后的最高温度,反应后温度不一定为最高温度,故B错误;
C.碳生成稳定氧化物为二氧化碳,不是一氧化碳,所以不能表示碳的燃烧热,故C错误;
D.因为浓硫酸稀释放热,所以将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3kJ,故D错误;
故选:A.
点评 本题考查了燃烧热,和中和热的概念,熟悉二者概念是解题关键,注意浓硫酸稀释放出热量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列各组微粒均为正四面体结构,且仅含极性键的是( )
| A. | C2H2、BeCl2 | B. | SiCl4、NH4+ | C. | H2S、P4 | D. | CH4、BF3 |
7. 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
14.上海世博会开幕式于2010年4月30日顺利召开.世博会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图所示,下列关于该物质的说法正确的是( )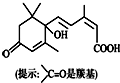

| A. | 其分子式为C15H22O4 | |
| B. | 一定条件下,l mol该有机物最多可与4 mol氢气发生加成反应 | |
| C. | 1 mol该物质与足量NaOH溶液反应,最多消耗2 mol NaOH | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
4.下列能说明氯的非金属性比硫强的事实是( )
①HCl比H2S稳定 ②HClO4酸性比H2SO4强 ③Cl2能与H2S反应生成S.
①HCl比H2S稳定 ②HClO4酸性比H2SO4强 ③Cl2能与H2S反应生成S.
| A. | ②③ | B. | ①② | C. | ①③ | D. | ①②③ |
11.下列电子式书写正确的是( )
| A. | 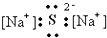 | B. |  | C. |  | D. |  |
8.下列物质中含有共价键的离子化合物是( )
| A. | KOH | B. | MgCl2 | C. | CO2 | D. | CH4 |
9. 合成氨反应:N2+3H2?高温、高压催化剂?高温、高压催化剂2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2?高温、高压催化剂?高温、高压催化剂2NH3 △H=-92.4kJ•mol.
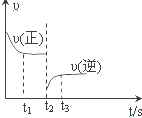
如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
 合成氨反应:N2+3H2?高温、高压催化剂?高温、高压催化剂2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2?高温、高压催化剂?高温、高压催化剂2NH3 △H=-92.4kJ•mol.如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
| A. | 升高温度 | B. | 分离出部分氨气 | C. | 降低压强 | D. | 增大反应物浓度 |

 .
.