��Ŀ����
3��X��Y��Z��W��ԭ���������������ǰ������Ԫ�أ�X�������ܼ����Ų��ĵ�������ȣ�Y��̬ԭ�ӵ�δ�ɶԵ��������ܼ�����ȣ�Zλ��X�����������ڣ�����������ݷֱ��ǣ�I1=419kJ•mol-1��I2=3051kJ•mol-1��I3=4411kJ•mol-1��W3+�ĺ�������Ų�ʽ��[Ar]3d5���ش��������⣺��1��X��Y��Z����Ԫ�ص縺���ɴ�С��˳��ΪN��C��K��
��2��X��ij����������Y2��Ϊ�ȵ����壬д����������Ľṹ��ʽC��O���������������Ļ�ѧ�������ǹ��ۼ���
��3��YH4+�Ŀռ乹�����������壮Xԭ�ӵ��ӻ���ʽ��Ϊsp2����Է���������С��X���⻯�����ʽΪC2H4��
��4������Ԫ�ؿ��γɻ�����Z4[W��XY��n]��Wԭ�ӵ������������������γ���λ��ʱ�ṩ�ĵ�����֮��Ϊ14���� n=6��
��5����ͼB ���A������B����C������ʾ����Z���������Ķѻ���ʽ����Z������һ�������ı߳�Ϊa pm����Z������ܶ�Ϊ$\frac{78}{��a��1{0}^{-10}��^{3}•{N}_{A}}$g/m3��д����a�ı���ʽ����NA��ʾ����٤����������

���� X��Y��Z��W��ԭ���������������ǰ������Ԫ�أ�X�������ܼ����Ų��ĵ�������ȣ���Xԭ�ӵĺ�������Ų�Ϊ1s22s22p2����XΪCԪ�أ�Y��̬ԭ�ӵ�δ�ɶԵ��������ܼ�����ȣ���ԭ����������X����Y����3���ܼ�����Zλ��X�����������ڣ�����Ԫ�ض���ǰ������Ԫ�أ���Yֻ�ܴ��ڵڶ����ڡ�X���ڵ������ڣ���Y��δ�ɶԵ�����Ϊ3�����������Ų�Ϊ1s22s22p3����YΪNԪ�أ�W3+�ĺ�������Ų�ʽ��[Ar]3d5����Wԭ�ӵļ۵����Ų�ʽΪ3d64s2����WΪ26��FeԪ�أ�Z���ڵ������ڣ������������Ϊ��I1=419kJ•mol-1��I2=3051kJ•mol-1��I3=4411kJ•mol-1��˵��Z����㺬��1�����ӣ�ԭ������С��Fe����ZΪKԪ�أ��ݴ˽��н��
��� �⣺X��Y��Z��W��ԭ���������������ǰ������Ԫ�أ�X�������ܼ����Ų��ĵ�������ȣ���Xԭ�ӵĺ�������Ų�Ϊ1s22s22p2����XΪCԪ�أ�Y��̬ԭ�ӵ�δ�ɶԵ��������ܼ�����ȣ���ԭ����������X����Y����3���ܼ�����Zλ��X�����������ڣ�����Ԫ�ض���ǰ������Ԫ�أ���Yֻ�ܴ��ڵڶ����ڡ�X���ڵ������ڣ���Y��δ�ɶԵ�����Ϊ3�����������Ų�Ϊ1s22s22p3����YΪNԪ�أ�W3+�ĺ�������Ų�ʽ��[Ar]3d5����Wԭ�ӵļ۵����Ų�ʽΪ3d64s2����WΪ26��FeԪ�أ�Z���ڵ������ڣ������������Ϊ��I1=419kJ•mol-1��I2=3051kJ•mol-1��I3=4411kJ•mol-1��˵��Z����㺬��1�����ӣ�ԭ������С��Fe����ZΪKԪ�أ�
��1��X��Y��Z�ֱ�Ϊ��C��N��K������Ԫ�صĵ縺��С�ڷǽ�����ͬһ������ԭ������Խ�縺��Խǿ��������Ԫ�ص縺���ɴ�С��˳��Ϊ��N��C��K��
�ʴ�Ϊ��N��C��K��
��2��Y2ΪN2������14�����ӣ�XΪCԪ�أ�C����������N2Ϊ�ȵ����壬��������ΪCO����ṹ�뵪�����ƣ�����CO�ĽṹʽΪ��C��O��COΪ���ۻ���������к��й��ۼ���
�ʴ�Ϊ��C��O�����ۼ���
��3��YH4+ΪNH4+������ԭ��Nԭ���γɵ�4�����ۼ���Ϊsp3�ӻ����ռ乹��Ϊ��������ṹ��Cԭ�ӵ��ӻ���ʽ��Ϊsp2����C�γ���2��������1��˫����������������Է���������С��X���⻯��Ϊ��ϩ������ʽΪ��C2H4��
�ʴ�Ϊ���������壻C2H4��
��4������Ԫ�ؿ��γɻ�����Z4[W��XY��n]ΪK4[Fe��CN��n]��Wԭ�ӵ������������������γ���λ��ʱ�ṩ�ĵ�����֮��Ϊ14������Feԭ�������Ϊ2�����ӣ��������γ���λ��ʱ�ṩ�ĵ�����Ϊ��14-2=12������n=6��
�ʴ�Ϊ��6��
��5��ZΪKԪ�أ�������Ϊ���������ѻ���������ȷ�ѻ���ʽΪB��ÿ�������к��м�ԭ����ĿΪ��8��$\frac{1}{8}$+1=2��ÿ������������Ϊ��2��$\frac{39}{{N}_{A}}$�����������Ϊ��V=��apm��3=��a��10-10��m3�����Լ�����ܶ�Ϊ����=$\frac{m}{V}$=$\frac{\frac{78}{{N}_{A}}g}{��a��1{0}^{-10}{��^{3}m}^{3}}$=$\frac{78}{��a��1{0}^{-10}��^{3}•{N}_{A}}$g/m3��
�ʴ�Ϊ��B��$\frac{78}{��a��1{0}^{-10}��^{3}•{N}_{A}}$g/m3��
���� ���⿼����λ�á��ṹ�����ʹ�ϵ���ۺ�Ӧ�á������ļ��㣬��Ŀ�Ѷ��еȣ������ƶϸ�Ԫ��Ϊ���ؼ���ע������Ԫ�����ڱ��ṹ��Ԫ�������ɵ����ݣ���ȷ������������ѻ���ʽ������֪ʶ��϶࣬�ۺ��Խ�ǿ����ֿ�����ѧ�����Ӧ�û���֪ʶ��������

| ѡ�� | ʵ����� | ʵ��Ŀ�Ļ���� |
| A | ��������FeCl3��MgCl2��Һ�м�������Mg��OH��2��ĩ������һ��ʱ������ | ��ȥMgCl2��Һ������FeCl3 |
| B | ��ij��Һ�м���BaCl2��Һ���ɰ�ɫ������������ϡ�����������ʧ | ֤����Һ�к�SO42- |
| C | ��ij��Һ�м���ϡ���ᣬ�ų���ɫ��ζ���壬������ͨ�����ʯ��ˮ��ʯ��ˮ����� | ֤������Һ�д���CO32- |
| D | ��֧�Թ���װ�е��������Ũ�ȵ�H2O2��Һ��������һ֧�Թ��м���FeCl3��Һ | FeCl3��Һ��H2O2�ֽ�������Ӱ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
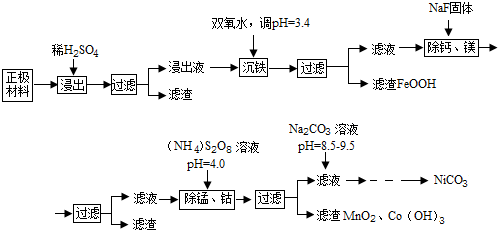
��֪���ٽ���Һ�и����Ӻ���
| �������� | Ni2+ | Co2+ | Fe3+ | Mn2+ | Ca2+ | Mg2+ |
| Ũ�ȣ�g/L�� | 63.6 | 5.90 | 1.00 | 0.22 | 5.24��10-2 | 6.37��10-2 |
�ش��������⣺
��1������Һ���������У����ɵij�����FeOOH��������Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H2O=2FeOOH+4H+
��2������NaF�ɳ�ȥCa2+��Mg2+����ʹ��Һ��Ca2+��Mg2+Ũ��С��1.0��10-5mol/L��FŨ�ȱ������$\sqrt{\frac{6.5��1{0}^{-9}}{1.0��1{0}^{-5}}}$mol/L���г�����ʽ���ɣ�
��3���������[��NH4��2S2O8���̵�ԭ���ǣ���һ���ù�����什���Һ�е�Mn2+������MnO4-���ڶ���MnO4-������Mn2-��Ӧ����MnO2�������ڵ�һ����Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ5��2���ڶ���������Ӧ�����ӷ���ʽΪ3Mn2++2MnO4-+2H2O=5MnO2��+4H+������ȥ1L����Һ�е�Mn2+��Co2+������Ҫ�������13.68g
��4�����̡���ʱ����ҺpH�ϴ���ʲô�����Ni2+Ҳ���γ�Ni��OH��2��������
��5������Na2CO3��Һ��Ϊ�õ�������NiCO3���壬��Ҫ�IJ����й��ˡ�ϴ�ӡ����
| ������ ��� | V��0.20mol/L H2C2O4��Һ��/mL | �� | V��O��O1mol/L KMnO4��Һ��/mL | M��MnSO4���壩/g | T/�� | �� |
| �� | 2.0 | 0 | 4.0 | 0 | 5.0 | |
| �� | 2.0 | 0 | 4.0 | 0 | 2.5 | |
| �� | 1.0 | a | 4.0 | 0 | 2.5 | |
| �� | 2.0 | 0 | 4.0 | 0.1 | 2.5 |
��1�����������Ӧԭ�������ӷ�Ӧ����ʽ
��MnO4-+��5H2C2O2+��6H+=��Mn2-+��CO2��+��H2
��2������ʵ��٢����¶�̽���Ի�ѧ��Ӧ���ʵ�Ӱ�죻������ʵ��ڢ���̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬������С��ס�Ӧ��дV������ˮ��/mL��aΪ1.0������ʵ����Ҫ��������������������С��ҡ�Ӧ��
д��Һ��ɫ��ʱ��
��3������ʵ��ڢ���̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���ڴ����������ͼ1�л����ںܵ͢������仯��ϵͼ������Ҫ�ı�ע��
��ij��ѧС������ͼ2װ�ý���ʵ��֤�������ԣ�KMnO4��Cl2��Br2����ѡ�Լ���KBr��Һ��KMnO4��Ũ���ᡢŨ����
��4��װ��a��d��ʢ�ŵ��Լ��ֱ��ǣ�Ũ���ᡢKBr��Һ�������й۲쵽������Ϊc���л���ɫ���������d����Һ��Ϊ�ػ�ɫ����ʵ��װ�õIJ���֮������β������װ��

| A�� | 22 | B�� | 23 | C�� | 24 | D�� | 25 |
| A�� | ��ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���NaNO3���壬ͭ���Բ��ܽ� | |
| B�� | ��������Һ�м��˹���NaOH��Һ�����������ɫ���� | |
| C�� | ��ȥFeCl3��������FeCl2�����˹���ϡ���� | |
| D�� | Ũ���ᡢŨ�����ڼ����������ܽ�ľ̿����Ϊ������̼ |

| A�� | ����������ʵ���Ũ��Ϊ9.2 mol/L | |
| B�� | 1 mol Zn�����������ᷴӦ����2 g���� | |
| C�� | ����200 mL 4.6 mol/L��ϡ������ȡ������50 mL | |
| D�� | ���������������ˮ��Ϻ�������Һ��Ũ�ȴ���9.2 mol/L |


 $��_{��}^{KMnO_{4}/H+}$
$��_{��}^{KMnO_{4}/H+}$
 ��
�� ��
��