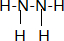题目内容
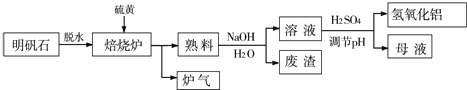
13.已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol 丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件巳略去).
用化学用语回答下列问题:
(1)单质B的组成元素在周期表中的位置是第2周期第ⅤA族、NaClO中对应元素的离子半径由大到小顺序为:Cl->O2->Na+.
(2)戊与强碱反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(3)丁中所包含的化学键有极性共价键和非极性共价键.
(4)反应①的化学方程式为N2+3H2$?_{高温高压}^{催化剂}$2NH3.
(5)反应②中,0.5mol NaClO参加反应时,转移1mol电子,其化学方程式为2NH3+NaClO═N2H4+NaCl+H2O.
(6)-定条件下,A与Ti O2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分.已知,该反应生成1mol乙时放出536kJ热量,其热化学方程式为4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1072kJ/mol.
分析 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体,则丙为NH3;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子,则丁为N2H4;戊是一种难溶于水的白色胶状物质,既能与强酸反应也能与强碱反应,具有净水作用,则戊为Al(OH)3;结合转化关系图可知,乙为氧化铝,A为Al;B为N2,甲为氮化铝,D为H2,然后结合物质的性质及化学用语来解答.
解答 解:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体,则丙为NH3;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子,则丁为N2H4;戊是一种难溶于水的白色胶状物质,既能与强酸反应也能与强碱反应,具有净水作用,则戊为Al(OH)3;结合转化关系图可知,乙为氧化铝,A为Al;B为N2,甲为氮化铝,D为H2,
(1)组成B的元素为N元素,位于元素周期表中第2周期第ⅤA族,离子核外电子层数越多,半径越大,电子层数相同时,核电荷数越大,半径越小,所以NaClO中对应元素的离子半径由大到小顺序为Cl->O2->Na+,
故答案为:第2周期第ⅤA族;Cl->O2->Na+;
(2)戊为Al(OH)3,戊与强碱反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(3)丁为N2H4,含有N-H极性共价键和N-N非极性共价键,
故答案为:极性共价键和非极性共价键;
(4)反应①为合成氨的反应,即N2+3H2$?_{高温高压}^{催化剂}$2NH3,
故答案为:N2+3H2$?_{高温高压}^{催化剂}$2NH3;
(5)反应②为氨气与NaClO的反应,0.5molNaClO参加反应时,转移1mol电子,则Cl元素由+1价降低为-1价,该反应生成NaCl,同时生成N2H4和水,则该反应为2NH3+NaClO═N2H4+NaCl+H2O,
故答案为:2NH3+NaClO═N2H4+NaCl+H2O;
(6)-定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),即Al、TiO2、C反应生成Al2O3、TiC,生成1molAl2O3时放出536kJ热量,则生成2molAl2O3时放出536kJ×2=1072kJ的热量,所以热化学反应方程式为4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1072kJ/mol,
故答案为:4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1072kJ/mol.
点评 本题考查无机物的推断,物质的推断是解答本题的关键,丙、戊为解答本题的突破口,并熟悉化学用语的使用来解答即可,题目难度中等.

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
| A. | 再投入2molA和1molB | B. | 保持体积不变通入1molB | ||
| C. | 移出部分物质B | D. | 再投入2molA,1molB和0.6molD |
| A. | C2H4Cl2 | B. | C2H3Cl3 | C. | C2HCl3 | D. | C2H2Cl2 |
①除去乙烷中少量的乙烯:催化条件下通入H2;②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏;③除去C2H4中少量的SO2:气体通过盛氢氧化钠溶液的洗气瓶;④除去乙醇中少量的水:加足量生石灰,蒸馏.
| A. | ①②④ | B. | ②④ | C. | ①③④ | D. | ③④ |
| A. | 冰箱中使用的含氟制冷剂泄露后,会增加空气中的PM2.5 | |
| B. | 节日焰火的五彩缤纷是某些金属单质性质的体现 | |
| C. | 施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用 | |
| D. | 化学反应能够制造出新的物质,同时也能制造出新的元素 |