题目内容
17.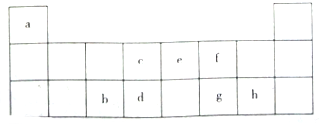 如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:(1)上述所列元素中,最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(2)d、e、f三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)SiH4<NH3<H2O.
(3)a、c两种元素可形成多种化合物,其中化合物A的产量是衡量一个国家石油化工发展水平的标志,则:
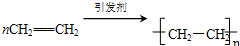
①A的结构简式为CH2=CH2;以A为原料,可制得当今世界上产量最大的塑料产品,该反应的化学方程式为
 ;
;②A可与H2O反应生成化合物CH3CH2OH该反应类型为加成反应.CH3CH2OH与CH3COOH反应生成有果香气味的产物,该反应的化学方程式为CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(4)元素e的气态氢化物与其最高价氧化物的水化物反应生成的物质为NH4NO3(用化学式表示),该物质所含化学键类型为离子键、共价键,属于离子化合物(填“离子”或“共价”).
分析 根据元素所在周期表中的位置可知a为H元素,b为Al元素,c为C元素,d为Si元素,e为N元素,f为O元素,g为S元素,h为Cl元素,结合元素周期律的递变规律以及对应物质的性质进行分析.
解答 解:根据元素所在周期表中的位置可知a为H元素,b为Al元素,c为C元素,d为Si元素,e为N元素,f为O元素,g为S元素,h为Cl元素,
(1)HClO4是酸性最强的无机含氧酸,
故答案为:HClO4;
(2)非金属性越强氢化物越稳定,由元素在周期表的位置可知,非金属性Si<N<O,故氢化物稳定性SiH4<NH3<H2O,
故答案为:SiH4<NH3<H2O;
(3)H、C两种元素可形成多种化合物,化合物A的产量是衡量一个国家石油化工发展水平的标志,则A为乙烯,
①A的结构简式为CH2=CH2,乙烯发生加聚反应得到聚乙烯,方程式为: ,
,
故答案为:CH2=CH2; ;
;
②乙烯与水发生加成反应生成的B,B为CH3CH2OH,以乙酸反应生成乙酸乙酯,方程式为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:加成反应;CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(4)元素e的气态氢化物与其最高价氧化物的水化物反应生成的物质为NH4NO3,属于离子化合物,含有离子键、共价键,
故答案为:NH4NO3;离子键、共价键;离子.
点评 本题考查结构性质位置关系、元素周期律、有机物的推断与性质、元素化合物性质等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
8.下列有关胶体的叙述正确的是( )
| A. | 胶体粒子的大小通常在0.1~1nm之间 | |
| B. | 阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现 | |
| C. | 可以通过过滤分离溶液和胶体 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体 |
2.有七种物质:①甲烷、②苯、③聚乙烯、④戊二烯、⑤2-丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ②③④⑤ | B. | ④⑤⑦ | C. | ①③④⑤ | D. | ④⑤⑥⑦ |
9.已知在干冰晶胞中每个顶角各有1个CO2分子,每个面心各有一个CO2分子.实验测得25℃时干冰晶体的晶胞边长为a cm,其摩尔质量为M g/mol,则该干冰晶体的密度为(单位:g/cm3)( )
| A. | $\frac{4M}{{a}^{3}}$ | B. | $\frac{M}{{a}^{3}{N}_{A}}$ | C. | $\frac{2M}{{a}^{3}{N}_{A}}$ | D. | $\frac{4M}{{a}^{3}{N}_{A}}$ |
7.在密闭容器中充入4mol X,在一定温度下4X(g)?3Y(g)+Z(g),达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是( )
| A. | 3.4 mol | B. | 4 mol | C. | 2.8 mol | D. | 1.2 mol |