题目内容
7.在密闭容器中充入4mol X,在一定温度下4X(g)?3Y(g)+Z(g),达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是( )| A. | 3.4 mol | B. | 4 mol | C. | 2.8 mol | D. | 1.2 mol |
分析 观察反应可知,反应前后气体的物质的量相等,所以,平衡时气体的物质的量不变,由此分析解答.
解答 解:反应前后气体的物质的量相等,所以,平衡时混合气体的物质的量不变为4mol,故选B.
点评 本题考查化学平衡的计算,题目难度不大,计算时注意气体体积前后不变的反应,无论反应是否达到平衡状态,混合气体的物质的量不变.

练习册系列答案
相关题目
15.X元素的阳离子和Y元素的阴离子的核外电子层结构相同,下列叙述正确的是( )
| A. | 离子半径X>Y | B. | 原子半径X<Y | ||
| C. | 原子序数X<Y | D. | 原子最外层电子数X<Y |
12.下列有关胶体的说法正确的是( )
| A. | 胶体都是均匀透明的液体 | |
| B. | 胶体粒子能透过半透膜而溶液不能 | |
| C. | 胶体与溶液的本质区别在于粒子直径的大小不同 | |
| D. | 利用丁达尔效应可区别浊液和胶体 |
16.下列反应中不属于可逆反应的是( )
| A. | SO2溶于水和H2SO3分解 | |
| B. | H2跟I2化合成HI和HI分解 | |
| C. | SO2跟O2化合成SO3和SO3分解 | |
| D. | 电解水生成H2与O2和H2与O2转化成H2O |
17.SO2是造成大气污染的主要气体,造成大气中SO2含量增加最主要原因是( )
| A. | 实验室排放的SO2 | B. | 火山爆发产生的SO2 | ||
| C. | 燃烧煤和石油产品产生的SO2 | D. | 工业制硫酸排放的SO2 |
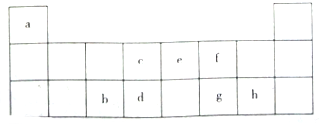 如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题: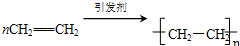 ;
;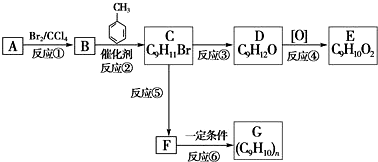
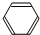 +CH3Br$\stackrel{催化剂}{→}$
+CH3Br$\stackrel{催化剂}{→}$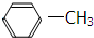 -CH3+HBr;
-CH3+HBr;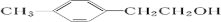 .
.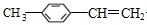 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$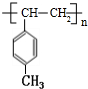 .
. +
+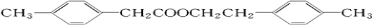 .
.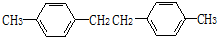 .
.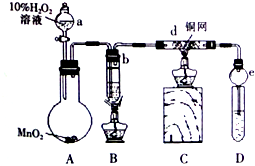 某校课外活动小组的同学在完成课本乙醇氧化制乙醛的实验后,改进了实验方案(如图),进行如下实验操作(顺序已打乱):
某校课外活动小组的同学在完成课本乙醇氧化制乙醛的实验后,改进了实验方案(如图),进行如下实验操作(顺序已打乱):