题目内容
【题目】以辉铜矿(Cu2S)为原料冶炼铜,其反应原理可表示为Cu2S+O2![]() 2Cu+SO2。下列说法不正确的是( )
2Cu+SO2。下列说法不正确的是( )
A.化合价发生变化的元素有3种
B.Cu2S在该反应中既是氧化剂又是还原剂
C.1 mol O2参加反应时,上述反应转移电子总物质的量为4 mol
D.SO2被分离、回收后氧化生成SO3,作为制取硫酸的原料
【答案】C
【解析】
A.该反应Cu2S+O2 ![]() 2Cu+SO2中,硫元素化合价由-2价变为+4价,氧元素化合价由0价变为-2价,铜元素化合价由+1价变为0价,所以化合价发生变化的元素是3种,故A正确;
2Cu+SO2中,硫元素化合价由-2价变为+4价,氧元素化合价由0价变为-2价,铜元素化合价由+1价变为0价,所以化合价发生变化的元素是3种,故A正确;
B.该反应中硫元素化合价由-2价变为+4价,铜元素化合价由+1价变为0价,所以Cu2S既是氧化剂又是还原剂,故B正确;
C.铜元素化合价从+1价变化为0价,硫元素化合价从-2价变化为+4价,氧元素化合价从 0价变化为-2价,依据电子守恒得到:当1molO2参加反应时,共转移6mole-,故C错误;
D.二氧化硫被分离、回收后氧化生成SO3,三氧化硫和水反应生成硫酸,所以可以作为制取硫酸的原料,故D正确;
故答案为C。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
【题目】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
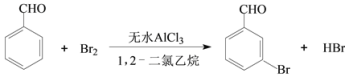
已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
沸点/℃ | 58.8 | 179 | 83.5 | 229 |
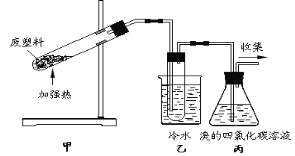
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如右图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。

步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出
MgSO4nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1)实验装置中冷凝管的主要作用是_____,锥形瓶中应为_____(填化学式)溶液。
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)_______。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3)步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的___(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是_____。
(5)步骤4中采用减压蒸馏,是为了防止______。
(6)若实验中加入了5.3 g苯甲醛,得到3.7 g间溴苯甲醛。则间溴苯甲醛产率为______。