题目内容
20.某主族元素的最高价氧化物的水化物的化学式是HRO3,则该元素的气态氢化物的化学式是( )| A. | HR | B. | H2R | C. | RH4 | D. | RH3 |
分析 化合物中元素的化合价代数和为零,据此计算R元素的最高化合价,再利用最高正化合价+|最低负化合价|=8,计算R元素在气态氢化物中的化合价,可确定氢化物化学式.
解答 解:元素R的最高价含氧酸的阴离子是RO3-,可知R的最高正价为+5价,则最低负化合价为5-8=-3,所以氢化物的化学式应为RH3,故选C.
点评 本题考查化合物中元素化合价的计算,难度不大,清楚化合物中元素的化合价代数和为零是关键,掌握识记常见元素的化合价.

练习册系列答案
相关题目
17.1995年化学家合成了一种分子式为C200H200的含多个碳碳三键的链状烃,其分子中碳碳三键最多可以是( )
| A. | 49个 | B. | 50个 | C. | 51个 | D. | 102个 |
15.下列与金属腐蚀有关的说法,正确的是( )
| A. | 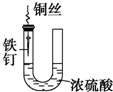 铁钉易被腐蚀 | |
| B. | 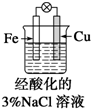 滴加少量KSCN溶液,溶液变为血红色 | |
| C. | 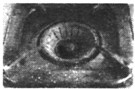 燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. |  用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极 |
5.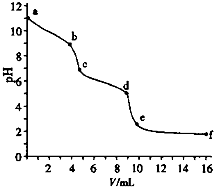 用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知:饱和CO2溶液pH为5.6),下列说法正确的是( )
用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知:饱和CO2溶液pH为5.6),下列说法正确的是( )
 用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知:饱和CO2溶液pH为5.6),下列说法正确的是( )
用已知浓度的盐酸滴定未知浓度的Na2CO3溶液.用 pH传感器测得混合溶液的pH变化曲线如图(已知:饱和CO2溶液pH为5.6),下列说法正确的是( )| A. | a处发生的离子反应:CO32-+H2O=HCO3-+OH- | |
| B. | 在pH=6时,c(Na+)>c(HCO3-)>c(CO32-) | |
| C. | 在pH=7时,c(Na+)=c(Cl-) | |
| D. | c→d发生的主要离子反应:CO32-+H+=HCO3- |
12.下列有关气体体积的叙述中,正确的是( )
| A. | 一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定. | |
| B. | 气体摩尔体积是指1摩尔任何气体所占的体积约为22.4L. | |
| C. | 不同的气体,若体积不同,则它们所含的分子数也不同 | |
| D. | 一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定 |

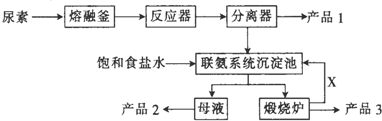
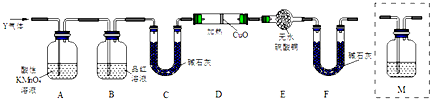
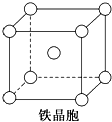 叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为:
叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为: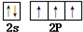 .
. ,
,