题目内容
9.甲同学设计并进行了如下实验,以探究乙炔与溴的加成反应:先取一定量工业用电石与水反应,将生成的气体通入足量的溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色的溶液里有少许黄色浑浊,推测在制得乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去杂质,再与溴水反应.请你回答下列问题:(1)写出甲同学实验中的两个化学方程式:CaC2+2H2O→Ca(OH)2+C2H2↑、CH≡CH+2Br2→CHBr2-CHBr2.
(2)乙认为甲设计的实验不能验证此反应为加成反应,其理由是CD.
A.使溴水褪色的物质,就是乙炔
B.使溴水褪色的反应就是加成反应
C.使溴水褪色的物质,未必是乙炔
D.使溴水褪色的反应未必是加成反应
(3)乙同学推测此乙炔中必定含有的一种杂质气体是H2S,在验证过程中必须全部除去,它与溴水反应的化学方程式是Br2+H2S=S↓+2HBr.
(4)请你选用下列三个装置(见图)(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品.
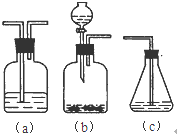
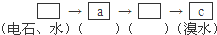 (填字母符号)
(填字母符号)(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证.
分析 (1)碳化钙能与水反应生成乙炔,乙炔具有不饱和键,能与溴水发生加成反应而使溴水褪色;
(2)生成的乙炔中混有硫化氢气体,可与溴水发生氧化还原反应而使溴水褪色;
(3)电石中含有硫化物,与水反应生成硫化氢气体,硫化氢具有还原性,溴水具有氧化性;
(4)实现乙同学的方案应用硫酸铜溶液除去硫化氢并检验是否完全除尽,之后再用溴水检验是否生成乙炔;
(5)根据取代反应的特征是:“有去有回”来回答.
解答 解:(1)碳化钙能与水反应生成乙炔和水,反应方程式为CaC2+2H2O→Ca(OH)2+C2H2↑,乙炔具有不饱和键,能与溴水发生加成反应而使溴水褪色,反应方程式为CH≡CH+2Br2→CHBr2-CHBr2,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;CH≡CH+2Br2→CHBr2-CHBr2;
(2)生成的乙炔中混有硫化氢气体,可与溴水发生氧化还原反应而使溴水褪色,故答案为:CD;
(3)电石中含有硫化物,与水反应生成硫化氢气体,硫化氢气体具有还原性,能与溴水发生氧化还原反应生成硫和溴化氢,反应方程式为Br2+H2S═S↓+2HBr,故答案为:H2S;Br2+H2S═S↓+2HBr;
(4)实现乙同学的方案应用硫酸铜溶液除去硫化氢并检验是否完全除尽,之后再用溴水检验是否生成乙炔,
故答案为:b;硫酸铜溶液;a;硫酸铜溶液;
(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证;故答案为:如若发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证.
点评 本题考查了乙炔的制备和性质实验,题目难度不大,本题中注意乙炔的除杂和性质实验,注意与溴水反应的性质.

| A. | 汽油 | B. | 煤油 | C. | 柴油 | D. | 润滑油 |
| A. | 向烧碱溶液中通入少量的二氧化碳 2OH-+CO2=CO32-+H2O | |
| B. | 向氯化铝溶液中滴加过量浓氨水 Al3++3OH-═Al(OH)3↓ | |
| C. | 向水玻璃中通入少量二氧化碳 SiO32-+CO2+H2O=H2SiO3↓+CO32- | |
| D. | 铝与氢氧化钠溶液反应 2Al+2OH-+6H2O═2AlO2-+3H2↑ |
| A. | SO2使紫色石蕊溶液变红色:SO2+H2O=2H++SO32- | |
| B. | 利用NaOH溶液除去金属铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O | |
| C. | 向淀粉碘化钾溶液中加稀硫酸,在空气中放置一段时间后变蓝:4H++4I-+O2=2I2+2H20 | |
| D. | 用盐酸洗涤试管中的Cu(OH)2:Cu(OH)2+2H+=Cu2++2H2O |
| A. | 锌片做负极,锌发生氧化反应 | B. | 铜片做正极 | ||
| C. | 溶液中的pH值增大 | D. | 溶液中的H+向负极移动 |
| A. | Cl-的结构示意图 | B. | MgCl2的电子式为 | ||
| C. | CCl4的结构式是 | D. | 高氯酸的分子式为HClO |
| A. | X由四种元素组成 | B. | X是化合物 | C. | X中有水 | D. | X 很稳定 |