题目内容
【题目】过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq)CH3CO3H(aq)+H2O(l) △H=-13.7KJ/mol
(1)市售过氧乙酸的浓度一般不超过21%,原因是____ 。
(2)利用上述反应制备760 9 CH3CO3H,放出的热量为____kJ。
(3)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25 ℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数,数据如图2所示。
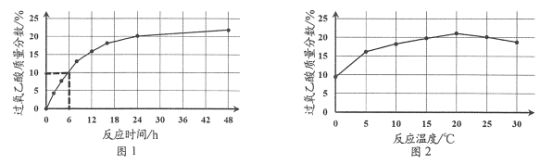
①实验1中,若反应混合液的总质量为mg,依据图1数据计算,在0—6h间,v(CH3CO3H)=____ g/h(用含m的代数式表示)。
②综合图1、图2分析,与20 ℃相比,25 ℃时过氧乙酸产率降低的可能原因是_________。(写出2条)。
(4) SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40 nm和70 nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。
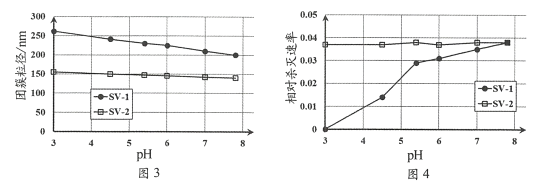
依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是______
【答案】高浓度易爆炸(或不稳定,或易分解) 137 0.1m/6 温度升高,过氧乙酸分解;温度升高,过氧化氢分解,过氧化氢浓度下降,反应速率下降 随着pH升高,SV-1的团簇粒径减小,与过氧化氢接触面积增大,反应速率加快
【解析】
(1)过氧乙酸(CH3CO3H)不稳定、易分解,高浓度易爆炸,为了安全市售过氧乙酸的浓度一般不超过21%
(2) 利用热化学方程式中各物质的系数代表各物质的物质的量来计算
(3) 结合图象分析计算
(1)市售过氧乙酸的浓度一般不超过21%,原因是不稳定、易分解,高浓度易爆炸。
(2) 利用热化学方程式中各物质的系数代表各物质的物质的量来计算。 利用上述反应制备760 g CH3CO3H,物质的量是10mol,所以放出的热量是方程式中反应热的10倍为137kJ。
(3) ①实验1中,若反应混合液的总质量为mg,依据图1数据计算,在0—6h间,v(CH3CO3H)=0.1
②综合图1、图2分析,与20 ℃相比,25 ℃时过氧乙酸产率降低的可能原因是温度升高,过氧乙酸分解;温度升高,过氧化氢分解,过氧化氢浓度下降,反应速率下降 。
(4)依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是随着pH升高,SV-1的团簇粒径减小,与过氧化氢接触面积增大,反应速率加快。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】如图所示装置中观察到电流计指针偏转,M棒变粗、N棒变细,以此判断下表中所列M、N、P物质,其中可以成立的是

选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸溶液 |
B | 铜 | 铁 | 稀盐酸溶液 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A.AB.BC.CD.D