题目内容
【题目】下列各组离子在指定溶液中,能大量共存的是( )
![]() 无色溶液中:
无色溶液中:![]()
![]()
![]()
![]()
![]()
![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 水电离的
水电离的![]() 浓度为
浓度为![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 加入铝粉放出氢气的溶液中:
加入铝粉放出氢气的溶液中:![]()
![]()
![]()
![]()
![]()
![]()
![]() 使甲基橙变红的溶液中:
使甲基橙变红的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 中性溶液中:
中性溶液中:![]()
![]()
![]()
![]()
![]() 能溶解铜粉的溶液:
能溶解铜粉的溶液:![]()
![]()
![]()
![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】D
【解析】
![]() 为橙色,与无色不符,故不符合题意;
为橙色,与无色不符,故不符合题意;
![]() 的溶液显碱性,该组离子之间不反应,可大量共存,故符合题意;
的溶液显碱性,该组离子之间不反应,可大量共存,故符合题意;
![]() 常温下水电离的
常温下水电离的![]() 浓度为
浓度为![]() 的溶液,水的电离被促进,溶液显酸性或碱性,酸性溶液中不能大量存在
的溶液,水的电离被促进,溶液显酸性或碱性,酸性溶液中不能大量存在![]() 、
、![]() ,碱性溶液中不能大量存在铵根离子,故不符合题意;
,碱性溶液中不能大量存在铵根离子,故不符合题意;
![]() 加入铝粉放出氢气的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在
加入铝粉放出氢气的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在![]() 、
、![]() ,酸性溶液中
,酸性溶液中![]() 不能大量存在,故不符合题意;
不能大量存在,故不符合题意;
![]() 使甲基橙变红的溶液显酸性,MnO4-、NO3-(H+)与Fe2+发生氧化还原反应,不能大量共存,故不符合题意;
使甲基橙变红的溶液显酸性,MnO4-、NO3-(H+)与Fe2+发生氧化还原反应,不能大量共存,故不符合题意;
![]() 中性溶液不能大量存在
中性溶液不能大量存在![]() 、
、![]() ,故不符合题意;
,故不符合题意;
![]() 能溶解铜粉的溶液,具有氧化性物质,不能存在还原性离子
能溶解铜粉的溶液,具有氧化性物质,不能存在还原性离子![]() ,且
,且![]() 、
、![]() 发生氧化还原反应,不能大量共存,故不符合题意;
发生氧化还原反应,不能大量共存,故不符合题意;
综上能大量共存的只有②;
故选D。

 阅读快车系列答案
阅读快车系列答案【题目】(1)用O2将HCl转化为Cl2,可提高效益,减少污染.传统上该转化通过如图所示的催化剂循环实现,其中,反应①为 2HCl(g)+CuO(s)=H2O(g)+CuCl2(s) ![]() 反应②生成1molCl2(g)的反应热为
反应②生成1molCl2(g)的反应热为![]() ,则总反应的热化学方程式为_______________(反应热△H用含
,则总反应的热化学方程式为_______________(反应热△H用含![]() 和
和![]() 的代数式表示)。
的代数式表示)。
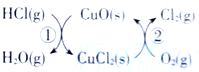
(2)在容积为1L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
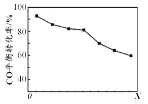
①该反应的![]() ____________0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如下表所示。在0~60s时段,反应速率υ(N2O4)为_________mol·L-1·s-1;40s时C2___________0.10mol/L(填“>”或“<”)。
____________0(填“>”或“<”);100℃时,体系中各物质浓度随时间变化如下表所示。在0~60s时段,反应速率υ(N2O4)为_________mol·L-1·s-1;40s时C2___________0.10mol/L(填“>”或“<”)。
②100℃时达平衡后,改变反应温度为![]() ,c(N2O4)以0.0020 mol·L
,c(N2O4)以0.0020 mol·L![]() ·s
·s![]() 的平均速率降低,经10s又达到平衡。则T______100℃(填“>”或“<”)。
的平均速率降低,经10s又达到平衡。则T______100℃(填“>”或“<”)。
③计算温度T时反应的平衡常数K___________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半。平衡向___________(填“正反应”或“逆反应”)方向移动,N2O4的转化率______(填“增大”或“减小”)。
时间(s) | 0 | 20 | 40 | 60 | 80 |
N2O4浓度 (mol/L) | 0.10 | 0.06 | C1 | 0.04 | 0.04 |
NO2浓度 (mol/L) | 0 | 0.08 | C2 | 0.12 | 0.12 |