题目内容
【题目】硫酸铜晶体(CuSO4·xH2O)是一种用途广泛的试剂。某小组拟探究硫酸铜晶体的性质。
实验I:探究硫酸铜的氧化性。
取适量硫酸铜溶液于试管中,加入(NH4)2SO3溶液,产生沉淀M。过滤、洗涤,得到固体M。为了探究M的组成,进行如下实验:
①将一定量同体M分成两份。
②在一份固体中加入稀硫酸,产生有刺激性气味的气体(X),溶液变成蓝色并有红色固体生成;将气体通入品红溶液中,品红溶液褪色。
③在另一份固体中加入浓烧碱溶液,共热,产生气体(Y),该气体能使湿润的红色石蕊试纸变蓝。回答下列问题:
(1)Y的电子式为_____________________。
(2)经测定M中阳离子、阴离子个数之比为2:1。M的化学式为__________。
实验II:探究硫酸铜晶体的热稳定性。
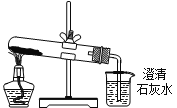
取少量硫酸铜晶体进行实验,装置如图所示。

己知部分实验现象为:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中产生白色沉淀;D中溶液变成红色。
(3)分析推测硫酸铜晶体的分解产物有_________________________。
(4)B、C装置的位置不能互换的原因是_______________________________________。
(5)D中的反应分两步进行,写出第一步反应的离子方程式_____________________。
【答案】 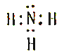 NH4CuSO3 CuO、SO3、SO2、O2、H2O 互换后,SO3溶于品红溶液,BaCl2溶液无法检出SO3 4Fe2++O2+4H+=4Fe3++2H2O
NH4CuSO3 CuO、SO3、SO2、O2、H2O 互换后,SO3溶于品红溶液,BaCl2溶液无法检出SO3 4Fe2++O2+4H+=4Fe3++2H2O
【解析】分析:I、在一份固体中加入稀硫酸,产生有刺激性气味的气体(X),溶液变成蓝色并有红色固体生成,说明有硫酸铜和单质铜生成;将气体通入品红溶液中,品红溶液褪色,气体是二氧化硫。
③在另一份固体中加入浓烧碱溶液,共热,产生气体(Y),该气体能使湿润的红色石蕊试纸变蓝,Y是氨气;
II、A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末,说明逐渐失去结晶水,最终变为氧化铜;B中产生白色沉淀,白色沉淀是硫酸钡,说明有三氧化硫产生;D中溶液变成红色,说明有铁离子生成,因此分解产物中有氧化性气体产生,结合物质的性质、氧化还原反应原理分析判断。
详解:(1)根据以上分析可知Y是碱性气体氨气,氨气是含有共价键的共价化合物,氨气的电子式为![]() 。
。
(2)根据以上分析可知M中的阳离子是铵根离子和亚铜离子,阴离子是亚硫酸根离子。经测定M中阳离子、阴离子个数之比为2:1,因此根据物质显电中性可知M的化学式为NH4CuSO3。
(3)根据以上分析可知分解产物中含有水蒸气、氧化铜、三氧化硫。具有氧化性的气体应该是氧气,氧气只能是氧化产物,则一定还存在还原产物二氧化硫,即硫酸铜晶体的分解产物有CuO、SO3、SO2、O2、H2O。
(4)由于互换后,SO3溶于品红溶液,BaCl2溶液无法检出SO3,所以B、C装置的位置不能互换。
(5)D中的反应分两步进行,第一步是氧气氧化亚铁离子,然后铁离子与KSCN溶液反应,则第一步反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O。

【题目】研究小组用如图装置制取Cl2 , 证明产生的气体中含有HCl. 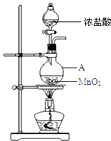
(1)仪器A的名称为;A中反应的离子方程式为;
(2)甲同学将A中产生的气体通入如表溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为;
②不能证明产生的气体中含有HCl的实验是(填字母序号);
(3)已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因;
(4)已知:2S2O32﹣+I2═S4O62﹣+2I﹣ . 丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2 . 取25.00mL溶液X,加入过量KI溶液,然后用0.04molL﹣1 Na2S2O3溶液滴定生成
的I2 , 达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl﹣ , 再用0.10molL﹣1 AgNO3溶液滴定所得溶液中的Cl﹣ .
①X中的HClO不会影响I的测定结果,原因是;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10molL﹣1 AgNO3溶液的体积应大于mL(用含V的代数式表示).