题目内容
【题目】MnCO3是信息产业和机电工业的重要基础功能材料,某地有含锰矿石(主要成分是MnO2还含CaO、Al2O3、FeS等杂质),由此矿石生产MnCO3的工艺流程如下:

回答下列问题:
(1)操作Ⅰ为:___________。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液pH所用物质X最好为(_______)
A.NaOH溶液 | B.氨水 | C.MnCO3固体 | D.盐酸 |
(4)滤渣Ⅰ为___________,滤渣Ⅱ为___________。
(5)沉锰的化学方程式为:______________________。
(6)MnCO3也是制造锂离子电池的重要原料,在此电池的正极,充放电过程中发生LiMn2O4与Li1-xMn2O4之间的转化,写出该电池充电时正极发生的反应式:________。
【答案】过滤 FeS + 12H++3MnO2![]() 2Fe3++ 2S↓ + 3Mn2++ 6H2O C Al(OH)3、Fe(OH)3CaF2 MnSO4+ 2NaHCO3=MnCO3+ Na2SO4+ H2O + CO2↑ LiMn2O4 -xe- =Li1-xMn2O4+ xLi+
2Fe3++ 2S↓ + 3Mn2++ 6H2O C Al(OH)3、Fe(OH)3CaF2 MnSO4+ 2NaHCO3=MnCO3+ Na2SO4+ H2O + CO2↑ LiMn2O4 -xe- =Li1-xMn2O4+ xLi+
【解析】
(1)操作Ⅰ得到单质S沉淀,所以操作为过滤;
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,说明有铁离子生成,所以酸溶过程中FeS发生反应的离子方程式为FeS + 12H++3MnO2![]() 2Fe3++ 2S↓ + 3Mn2++ 6H2O;
2Fe3++ 2S↓ + 3Mn2++ 6H2O;
(3)由于不能引入杂质,则调节溶液pH所用物质X最好为 MnCO3固体,答案选C;
(4)根据表中数据可知pH=6是铁离子、铝离子完全沉淀,则滤渣Ⅰ为Al(OH)3、Fe(OH)3;滤液中还含有钙离子,则加入NaF后转化为氟化钙沉淀,即滤渣Ⅱ为CaF2;
(5)沉锰的反应物是碳酸氢钠和硫酸锰,则反应的化学方程式为MnSO4+ 2NaHCO3=MnCO3+ Na2SO4+ H2O + CO2↑;
(6)电池充电时正极发生失去电子的氧化反应,则电极反应式为LiMn2O4 -xe- =Li1-xMn2O4+ xLi+;

【题目】某实验小组对KSCN的性质进行探究,设计如下实验:
试管中试剂 | 实验 | 滴加试剂 | 现象 |
| Ⅰ | ⅰ.先加1mL 0.1mol/L FeSO4溶液 ⅱ.再加硫酸酸化的KMnO4溶液 | ⅰ.无明显现象 ⅱ.先变红,后褪色 |
Ⅱ | ⅲ.先加1mL 0.05mol/L Fe2(SO4)3溶液 ⅳ.再滴加0.5mL 0.5mol/L FeSO4溶液 | ⅲ.溶液变红 ⅳ.红色明显变浅 |
(1)SCN-存在两种结构式,分别为N≡C-S-和S=C=N-,SCN-是二者的互变异构的混合物,请写出N≡C-S-的电子式__________________________。
(2)用离子方程式表示FeSO4溶液显酸性的原因______________________。
(3)①用离子方程式表示实验Ⅰ溶液变红的原因___________。
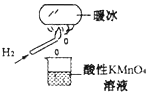
②针对实验Ⅰ中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如图实验装置证实了猜想是成立的。其中X溶液是_______,Y溶液是_______,检验产物SO42-的操作及现象是_____________________。

【题目】氨广泛用于生产化肥、制冷剂等方面。回答下列问题:
(1)实验室可用下图所示装置合成氨。

①合成氨时,还原铁粉的作用是________________。
②锥形瓶中盛有一定量的水,并滴有几滴酚酞试剂,反应—段时间后,锥形瓶中溶液变红,则气体X的成分为N2、水蒸气、____________和_________________。
⑵最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如图所示。

①图中反应Ⅱ的化学方程式为____________________。
②反应Ⅲ中能量转化的方式是__________________(填“电能转变为化学能”或“化学能转变为电能”)。
(3)液氨可用作制冷剂,液氨气化时__________(填“释放”或“吸收”)能量;液氨泄漏遇明火会发生爆炸。已知部分化学键的键能数据如下表所示:
共价键 | N-H | O=O | N≡N | O-H |
键能/kJ·mol-1 | 391 | 498 | 946 | 463 |
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应热△H=____________。