题目内容
【题目】某实验小组对KSCN的性质进行探究,设计如下实验:
试管中试剂 | 实验 | 滴加试剂 | 现象 |
| Ⅰ | ⅰ.先加1mL 0.1mol/L FeSO4溶液 ⅱ.再加硫酸酸化的KMnO4溶液 | ⅰ.无明显现象 ⅱ.先变红,后褪色 |
Ⅱ | ⅲ.先加1mL 0.05mol/L Fe2(SO4)3溶液 ⅳ.再滴加0.5mL 0.5mol/L FeSO4溶液 | ⅲ.溶液变红 ⅳ.红色明显变浅 |
(1)SCN-存在两种结构式,分别为N≡C-S-和S=C=N-,SCN-是二者的互变异构的混合物,请写出N≡C-S-的电子式__________________________。
(2)用离子方程式表示FeSO4溶液显酸性的原因______________________。
(3)①用离子方程式表示实验Ⅰ溶液变红的原因___________。
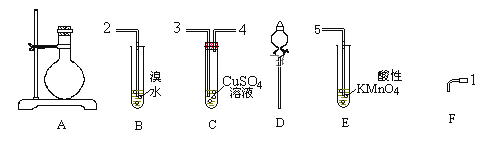
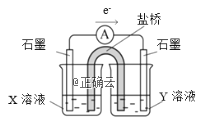
②针对实验Ⅰ中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如图实验装置证实了猜想是成立的。其中X溶液是_______,Y溶液是_______,检验产物SO42-的操作及现象是_____________________。
【答案】![]() Fe2++2H2O
Fe2++2H2O![]() Fe(OH)2+2H+ MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O Fe3++3SCN-
Fe(OH)2+2H+ MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O Fe3++3SCN-![]() Fe(SCN)3 0.1mol/L KSCN溶液,硫酸酸化的KMnO4溶液 一段时间后取少量反应后的KSCN溶液,先加盐酸酸化,再加氯化钡溶液,出现白色沉淀
Fe(SCN)3 0.1mol/L KSCN溶液,硫酸酸化的KMnO4溶液 一段时间后取少量反应后的KSCN溶液,先加盐酸酸化,再加氯化钡溶液,出现白色沉淀
【解析】
(1)根据结构式即可写电子式;
(2)考查盐类水解;
(3)探究溶液变红后褪色原因,先变红是Fe2+氧化为Fe3+,Fe3+再与 SCN-结合生成Fe(SCN)3;后褪色设计成原电池,从电子转移方向可判断正负极,结合化合价改变可判断电解质溶液。
(1)根据结构式N≡C-S-,可知电子式为![]() ;
;
(2)FeSO4是强酸弱碱盐,显酸性的原因是Fe2+的水解,离子方程式为:Fe2++2H2O![]() Fe(OH)2+2H+,
Fe(OH)2+2H+,
(3)①KMnO4将Fe2+氧化为Fe3+,Fe3+再与SCN-结合生成Fe(SCN)3,溶液变红,离子方程式为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,Fe3+ +3SCN-![]() Fe(SCN)3;
Fe(SCN)3;
②探究SCN-是否被酸性KMnO4氧化为SO42-,设计成原电池,由电子转移方向可知, X溶液所处电极为负极,化合价升高,失去电子,故X溶液是0.1mol/L KSCN溶液,Y溶液是硫酸酸化的KMnO4溶液;检验产物SO42-的操作及现象是:一段时间后取少量反应后的KSCN溶液,先加盐酸酸化,再加氯化钡溶液,出现白色沉淀。

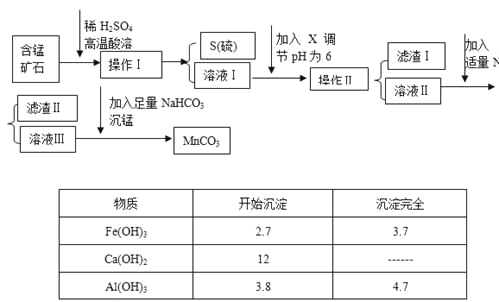
【题目】MnCO3是信息产业和机电工业的重要基础功能材料,某地有含锰矿石(主要成分是MnO2还含CaO、Al2O3、FeS等杂质),由此矿石生产MnCO3的工艺流程如下:
回答下列问题:
(1)操作Ⅰ为:___________。
(2)取溶液Ⅰ加入KSCN溶液,溶液呈血红色,试写出酸溶过程中FeS发生反应的离子方程式:
(3)调节溶液pH所用物质X最好为(_______)
A.NaOH溶液 | B.氨水 | C.MnCO3固体 | D.盐酸 |
(4)滤渣Ⅰ为___________,滤渣Ⅱ为___________。
(5)沉锰的化学方程式为:______________________。
(6)MnCO3也是制造锂离子电池的重要原料,在此电池的正极,充放电过程中发生LiMn2O4与Li1-xMn2O4之间的转化,写出该电池充电时正极发生的反应式:________。