题目内容
13.有机物F(Bisphenol A dimethacrylate)是一种交联单体.合成F的一种路线如下: ,
,已知以下信息:
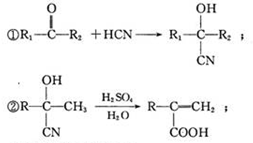
③B不能发生银镜反应;
④C能与FeCl3发生显色反应,核磁共振氢谱显示有4种不同化学环境的氢;
⑤E既能使溴水褪色又能使石蕊试液显红色.
回答下列问题:
(1)A与B反应生成C的化学方程式为
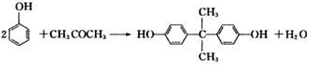 .
.(2)B→D的反应类型为加成反应,E的结构简式为CH2=C(CH3)COOH.
(3)1molF与足量NaOH溶液反应,最多消耗4molNaOH.
(4)C的同分异构体中含有萘环(
 )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是 (写出其中一种的结构简式).
(写出其中一种的结构简式).(5)A经如下步骤可合成环己烯甲酸:

反应条件1为催化剂、加热、加压,反应条件2为O2/Cu、△,反应条件3所选择的试剂为HCN,Ⅰ的结构简式为
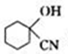 .
.
分析 根据分子式知,A为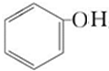 ,B中不饱和度=$\frac{3×2+2-6}{2}$=1,B不能发生银镜反应,则B为CH3COCH3,根据信息④知,C中不含酚羟基、且有4种氢原子,结合F结构简式知,C结构简式为
,B中不饱和度=$\frac{3×2+2-6}{2}$=1,B不能发生银镜反应,则B为CH3COCH3,根据信息④知,C中不含酚羟基、且有4种氢原子,结合F结构简式知,C结构简式为 ,根据信息①知,D结构简式为(CH3)2C(OH)CN,根据信息②知,E结构简式为CH2=C(CH3)COOH,
,根据信息①知,D结构简式为(CH3)2C(OH)CN,根据信息②知,E结构简式为CH2=C(CH3)COOH,
(5)苯酚和氢气在一定条件下发生加成反应生成环己醇,所以G为环己醇,环己醇被氧化生成环己酮,则H为环己酮,环己酮和HCN发生加成反应生成 ,所以I为
,所以I为 ,I水解生成环己烯甲酸,据此分析解答.
,I水解生成环己烯甲酸,据此分析解答.
解答 解:根据分子式知,A为 ,B中不饱和度=$\frac{3×2+2-6}{2}$=1,B不能发生银镜反应,则B为CH3COCH3,根据信息④知,C中不含酚羟基、且有4种氢原子,结合F结构简式知,C结构简式为
,B中不饱和度=$\frac{3×2+2-6}{2}$=1,B不能发生银镜反应,则B为CH3COCH3,根据信息④知,C中不含酚羟基、且有4种氢原子,结合F结构简式知,C结构简式为 ,根据信息①知,D结构简式为(CH3)2C(OH)CN,根据信息②知,E结构简式为CH2=C(CH3)COOH,
,根据信息①知,D结构简式为(CH3)2C(OH)CN,根据信息②知,E结构简式为CH2=C(CH3)COOH,
(5)苯酚和氢气在一定条件下发生加成反应生成环己醇,所以G为环己醇,环己醇被氧化生成环己酮,则H为环己酮,环己酮和HCN发生加成反应生成 ,所以I为
,所以I为 ,I水解生成环己烯甲酸,
,I水解生成环己烯甲酸,
(1)A为 ,B为CH3COCH3,A和B反应方程式为
,B为CH3COCH3,A和B反应方程式为 ,
,
故答案为: ;
;
(2)通过以上分析知,B发生加成反应生成D,E结构简式为CH2=C(CH3)COOH,
故答案为:加成反应;CH2=C(CH3)COOH;
(3)酯基水解生成的酚羟基、羧基能和NaOH所以,所以1molF与足量NaOH溶液反应,最多消耗4molNaOH,故答案为:4;
(4)C结构简式为 ,C的同分异构体中含有萘环(
,C的同分异构体中含有萘环( )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应说明含有酯基且酯基水解生成酚羟基,萘环上氢原子种类为2种,如果取代基为-OOCCH2CH2CH2CH3,有两种同分异构体;如果取代基为-OOCCH2CH(CH3)2,有两种同分异构体,如果取代基为-OOCCH(CH3)CH2CH3,有两种同分异构体,如果取代基为-OOCC(CH3)3有两种同分异构体,所以符合条件的一共8种;
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应说明含有酯基且酯基水解生成酚羟基,萘环上氢原子种类为2种,如果取代基为-OOCCH2CH2CH2CH3,有两种同分异构体;如果取代基为-OOCCH2CH(CH3)2,有两种同分异构体,如果取代基为-OOCCH(CH3)CH2CH3,有两种同分异构体,如果取代基为-OOCC(CH3)3有两种同分异构体,所以符合条件的一共8种;
其中核磁共振氢谱有8组峰的是 ,
,
故答案为:8; ;
;
(5)苯酚和氢气在催化剂、加热、加压条件下发生加成反应生成环己醇,所以G为环己醇,环己醇在Cu作催化剂、加热条件下被氧化生成环己酮,则H为H环己酮,环己酮和HCN发生加成反应生成 ,所以I为
,所以I为 ,I水解生成环己烯甲酸,所以反应条件1为催化剂、加热,反应条件2为氧气/Cu、加热,3为HCN,I的结构简式为
,I水解生成环己烯甲酸,所以反应条件1为催化剂、加热,反应条件2为氧气/Cu、加热,3为HCN,I的结构简式为 ,
,
故答案为:催化剂、加热、加压;O2/Cu、△; .
.
点评 本题考查有机物推断、有机物合成,侧重考查学生分析推断及知识迁移能力,由物质结构简式结合题给信息进行推断,难点是合成路线规划,要求学生要熟练掌握有机反应类型、官能团及其性质并灵活运用,题目难度中等.

| A. | 正反应的活化能比逆反应的活化能大234kJ•mol-1 | |
| B. | NO3是该反应的催化剂 | |
| C. | 化学反应速率v(NO2)=2v(CO) | |
| D. | 过程1和过程2均为放热反应 |
| A. | 乙烯(乙醇) | B. | 顺丁橡胶(石油裂解气) | ||
| C. | 碘(海带) | D. | 溴(海水晒盐后的余液) |
| A. | 矿物油和植物油都可以通过石油分馏来获取 | |
| B. | 硫酸亚铁可作补血剂组成成分 | |
| C. | 蛋白质的水解产物都是α-氨基酸 | |
| D. | 造成PM2.5的直接原因是土壤沙漠化 |
| A. | N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6KJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4kJ•mol-1 | |
| D. | CH4+2O2═CO2+2H2O△H=-890.3kJ•mol-1 |
 →CH3-CHO+H2O
→CH3-CHO+H2O
 ;F→H的反应类型是消去反应.
;F→H的反应类型是消去反应. .
. .
.