题目内容
18.某烷烃相对分子质量为86,如果分子中含有3个-CH2、2个-CH2-和一个-CH-,符合条件的该烃的结构式有(不考虑立体结构)( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 烷烃相对分子质量为86,则该烷烃含有的碳原子数目为:$\frac{86-2}{14}$=6,该烷烃为己烷;分子中含有3个-CH3、2个-CH2-和1个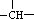 ,说明该烷烃只含有1个支链,其支链不可能为乙基,只能是甲基,据此判断即可.
,说明该烷烃只含有1个支链,其支链不可能为乙基,只能是甲基,据此判断即可.
解答 解:某烷烃相对分子质量为86,则该烷烃中含有碳原子数目为:N=$\frac{86-2}{14}$=6,为己烷;分子中含有3个-CH3、2个-CH2-和1个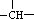 ,则该己烷分子中只能含有1个支链甲基,不会含有乙基,其主链含有5个C,满足条件的己烷的结构简式为:CH3CH(CH3)CH2CH2CH3,CH3CH2CH(CH3)CH2CH3,故选B.
,则该己烷分子中只能含有1个支链甲基,不会含有乙基,其主链含有5个C,满足条件的己烷的结构简式为:CH3CH(CH3)CH2CH2CH3,CH3CH2CH(CH3)CH2CH3,故选B.
点评 本题考查了同分异构体的求算,题目难度中等,注意掌握同分异构体的根据及求算方法与技巧,正确理解题干信息为解答本题的关键.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
8.根据热化学方程式,正确的是( )
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=-Q1 kJ•mol-1
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H2=-Q2 kJ•mol-1.
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=-Q1 kJ•mol-1
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H2=-Q2 kJ•mol-1.
| A. | Q1>Q2 | B. | △H1>△H2 | C. | Q1=Q2 | D. | △H1<△H2 |
9. 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
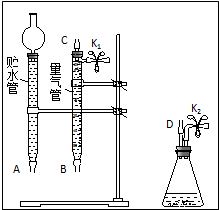
(1)现有以下仪器和用品:橡胶管、秒表、温度计、amol/L稀硝酸、bmol/L稀硝酸及下图中仪器.
①写出本实验的化学方程式,并标出电子转方向和数目: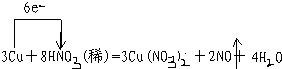 .
.
②设计实验方案:在相同稀硝酸浓度、不同温度(或相同温度、不同稀硝酸浓度)下,测定相同时间内产生气体体积(或产生相同体积的气体所需的时间).
③在答卷的图中将A、B、C、D、几处用橡胶管
以正确方式连接起来,以测定反应所产生气体的
体积(三个容器中的液体和水都已画出).
④测定前,为避免NO被氧化为NO2,要用CO2
排出锥形瓶和橡胶管中的空气:装入铜片、松开K2弹簧夹,从K2处的橡胶管向装置中通入CO2,此时K1处应进行的操作是松开K1弹簧夹,接导管通入澄清石灰水至出现白色浑浊为止.
(2)在K2处注入硝酸发生反应.在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间t1、t2、t3;收集气体体积V1、V2.请完成下表:
 某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.
某课外活动小组对“外界条件对铜与稀硝酸反应速率的影响”作了如下探究.(1)现有以下仪器和用品:橡胶管、秒表、温度计、amol/L稀硝酸、bmol/L稀硝酸及下图中仪器.
①写出本实验的化学方程式,并标出电子转方向和数目:
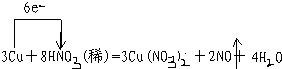 .
.②设计实验方案:在相同稀硝酸浓度、不同温度(或相同温度、不同稀硝酸浓度)下,测定相同时间内产生气体体积(或产生相同体积的气体所需的时间).
③在答卷的图中将A、B、C、D、几处用橡胶管
以正确方式连接起来,以测定反应所产生气体的
体积(三个容器中的液体和水都已画出).
④测定前,为避免NO被氧化为NO2,要用CO2
排出锥形瓶和橡胶管中的空气:装入铜片、松开K2弹簧夹,从K2处的橡胶管向装置中通入CO2,此时K1处应进行的操作是松开K1弹簧夹,接导管通入澄清石灰水至出现白色浑浊为止.
(2)在K2处注入硝酸发生反应.在给定条件下设计实验探究浓度和温度对化学反应速率的影响:温度25℃、50℃;时间t1、t2、t3;收集气体体积V1、V2.请完成下表:
| 实验 编号 | 稀硝酸的浓度/(mol/L) | 稀硝酸的体积/mL | 温度 /℃ | 时间 /min | 收集气体 的体积/mL |
| ① | a | V | 25 | t1 | V1 |
| ② | V | ||||
| ③ | V |
3.将木材隔绝空气加强热,可得到木煤气、木焦油和木炭等,这种加工方法化工生产中称为( )
| A. | 分馏 | B. | 裂化 | C. | 裂解 | D. | 干馏 |
10.某水体溶有Ca2+、Mg2+、HCO3-三种离子,可先加足量消石灰,再加足量纯碱以除去Ca2+、Mg2+.以下离子方程式肯定不符合反应事实的是( )
| A. | Mg2++2HCO3-+Ca2++2OH-→MgCO3↓+CaCO3↓+2H2O | |
| B. | Mg2++2HCO3-+2Ca2++4OH-→Mg(OH)2↓+2CaCO3↓+2H2O | |
| C. | Mg2++3HCO3-+3Ca2++5OH-→Mg(OH)2↓+3CaCO3↓+3H2O | |
| D. | Ca2++CO32-→CaCO3↓ |
7.在催化剂、400℃时可实现氯的循环利用,如图是其能量关系图,下列分析正确的是( )

| A. | 曲线a是使用了催化剂的能量变化曲线 | |
| B. | 反应物的总键能高于生成物的总键能 | |
| C. | 反应的热化学方程式为:4HCl(g)+O2(g)$→_{400℃}^{催化剂}$2Cl2+2H2O(g)-115.6 kJ | |
| D. | 若反应生成2mol液态水,放出的热量高于115.6kJ |
8.阿托酸乙酯可用于辅助胃肠道痉挛及溃疡.结构如图所示,下列说法正确的是( )
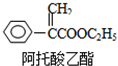

| A. | 能使高锰酸钾褪色,不能使溴水褪色 | |
| B. | 1mol阿托酸乙酯最多能与5mol H2加成 | |
| C. | 能发生加成、加聚、氧化、水解等反应 | |
| D. | 分子式为C11H13O2 |
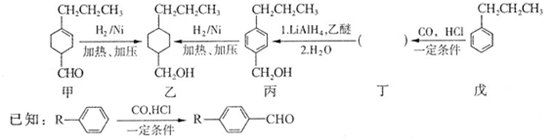
 和
和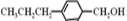 生成(写结构简式).
生成(写结构简式). .
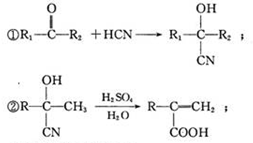
. +H2O$→_{△}^{NaOH}$
+H2O$→_{△}^{NaOH}$ +HCl或
+HCl或 ,
,
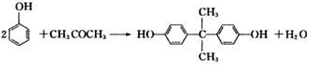 .
. )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是 (写出其中一种的结构简式).
(写出其中一种的结构简式).
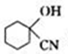 .
.