题目内容
3.下列热化学方程式书写正确的是(△H的绝对值均正确)( )| A. | N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6KJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4kJ•mol-1 | |
| D. | CH4+2O2═CO2+2H2O△H=-890.3kJ•mol-1 |
分析 A、△H的单位为mol/L;
B、氢气燃烧反应为放热反应;
C、N2H4燃烧反应为放热反应;
D、物质聚集状态未标注.
解答 解:A、△H的单位为mol/L,所以该热化学方程式应该为N2(g)+3H2(g)?2NH3(g)△H=-92.4mol/L,故A错误;
B、氢气燃烧反应为放热反应,焓变应为负值,所以该热化学方程式应该为2H2(g)+O2(g)═2H2O(l)△H=-571.6KJ•mol-1,故B错误;
C、N2H4燃烧反应为放热反应,所以该热化学方程式应该为N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4kJ•mol-1,故C正确;
D、热化学方程式应该标注各物质聚集状态,所以该热化学方程式应该为CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,故D错误;
故选C.
点评 本题考查了热化学方程式书写方法,注意热化学方程式书写方法和原则,题目难度中等.

练习册系列答案
相关题目
18.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Na+、Cl?、S2?、AlO2- | |
| B. | c(H+):c(OH-)=1:1012的溶液中Mg2+、Cu2+、Fe2+、SO42-、Cl?、NO3-可以大量共存 | |
| C. | pH=8的溶液中可能大量存在Na+、K+、Ba2+、Cl-、HCO3-、NO3- | |
| D. | 中性溶液中可能大量存在Fe3+、K+、Al3+、Cl-、SO42-、NO3- |
8.阿托酸乙酯可用于辅助胃肠道痉挛及溃疡.结构如图所示,下列说法正确的是( )
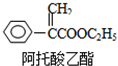

| A. | 能使高锰酸钾褪色,不能使溴水褪色 | |
| B. | 1mol阿托酸乙酯最多能与5mol H2加成 | |
| C. | 能发生加成、加聚、氧化、水解等反应 | |
| D. | 分子式为C11H13O2 |
 ,
,
 .
. )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的异构体共有8种(不考虑立体异构),其中核磁共振氢谱有8组峰的是 (写出其中一种的结构简式).
(写出其中一种的结构简式).
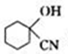 .
.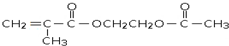 是锂电池正负极之间锂离子迁移的介质.由烃C4H8合成M的合成路线如图:
是锂电池正负极之间锂离子迁移的介质.由烃C4H8合成M的合成路线如图:
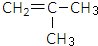 ,试剂II是NaOH水溶液.
,试剂II是NaOH水溶液.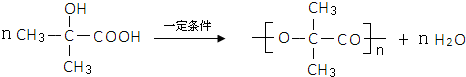 ;
;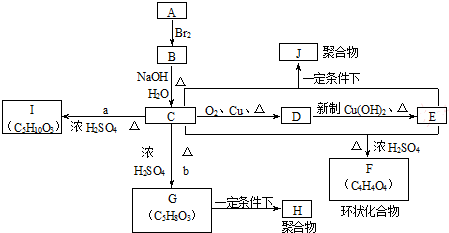
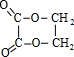 ;指出C→G的反应类型酯化(取代)反应.
;指出C→G的反应类型酯化(取代)反应.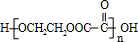 +(2n-1)H2O
+(2n-1)H2O