题目内容
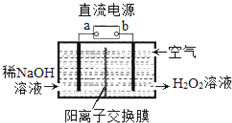
【题目】采用电化学法还原CO2是一种使CO2资源化的方法,如图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )

A. Pb与电源的正极相连
B. ZnC2O4在离子交换膜右侧生成
C. 正极反应式为:Zn﹣2e﹣═Zn2+
D. 标准状况下,当11.2 L CO2参与反应时,转移0.5mol电子
【答案】D
【解析】A、采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,A错误;B、在阴极上,二氧化碳得电子生成C2O42-,在阳极上,金属锌失电子成为锌离子,从阳极移向阴极,所以ZnC2O4在交换膜左侧生成,B错误;C、Zn是阳极不是正极,金属锌失电子成为锌离子,反应式为:Zn-2e-=Zn2+,C错误;D、电解的总反应为:2CO2+Zn ![]() ZnC2O4,2mol二氧化碳反应伴随2mol电子转移,当通入标况下的11.2 L CO2时,转移0.5 mol电子,D正确,答案选D。
ZnC2O4,2mol二氧化碳反应伴随2mol电子转移,当通入标况下的11.2 L CO2时,转移0.5 mol电子,D正确,答案选D。

练习册系列答案
相关题目