��Ŀ����
12���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺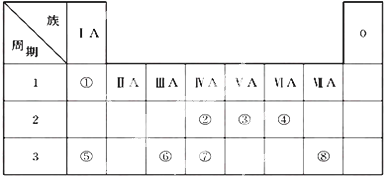
��1���ڴ�Ԫ�����ڱ���һ�����У���������ǿ��Ԫ����Na����Ԫ�ط��ţ�
��2���ݡ���ԭ�Ӱ뾶�ɴ�С��˳��ΪNa��Al����Ԫ�ط��ţ���
��3���ڡ��ۡ��ߵ���ۺ������������ǿ������˳����HNO3��H2CO3��H2SiO3 ���ѧʽ����
��4���١��ܡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ����д������һ�ֻ�����ĵ���ʽ��
 ��
��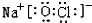 ��
����5���ɱ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬�������ϡ��Һ�ױ����ֽ⣬��ʹ�õĴ���Ϊ������ţ�ab��
a��MnO2 b��FeCl3 c��Na2SO3 d��KMnO4
��6���ɱ���Ԫ���γɵij�������X��Y��Z��M��N�ɷ������·�Ӧ��

X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪAl3++3NH3+3H2O=Al��OH��3��+3NH4+��N���ĵ��ʵĻ�ѧ����ʽΪ2Al2O3�����ڣ�$\frac{\underline{\;\;\;���\;\;\;}}{����ʯ}$ 4Al+3O2����
���� ��Ԫ�������ڱ��е�λ�ÿ�֪����ΪH����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪSi����ΪCl��
��1������ͬ����������ҽ����Լ�����ͬ�������϶��½�������ǿ��
��2��ͬ�����������ԭ�Ӱ뾶��С��
��3������ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ������ǽ�����Խǿ����ۺ����������Խǿ��
��4���١��ܡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ�������NaOH��NaClO�ȣ�
��5����������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬������ΪH2O2����MnO2��FeCl3�������·ֽ⣬��Na2SO3���л�ԭ�ԣ���H2O2����������ԭ��Ӧ��������ؾ���ǿ�����ԣ���H2O2����������ԭ��Ӧ��
��6��M�ǽ����ǽ������Σ�����Mһ������Σ�Z��N���ĵ��ʣ���ΪAl���ƶ�N����������Z���������������ݲ����Ϸ�Ӧ��X+Y+H2O��Al��OH��3+NH4+ ��֪���÷�ӦΪ���κ�һˮ�ϰ��ķ�Ӧ��
��� �⣺��Ԫ�������ڱ��е�λ�ÿ�֪����ΪH����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪSi����ΪCl��
��1������ͬ����������ҽ����Լ�����ͬ�������϶��½�������ǿ��������Ԫ����Na�Ľ�������ǿ���ʴ�Ϊ��Na��
��2��ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶��Na��Al���ʴ�Ϊ��Na��Al��
��3���ǽ����ԣ�N��C��Si��Ԫ�صķǽ�����Խǿ����Ӧ����ۺ����������Խǿ����HNO3��H2CO3��H2SiO3 ���ʴ�Ϊ��HNO3��H2CO3��H2SiO3 ��
��4���١��ܡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ�������NaOH��NaClO�ȣ���Ӧ�ĵ���ʽΪ�� ��
��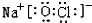 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��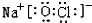 ��
��
��5������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬������ΪH2O2����MnO2��FeCl3�������·ֽ⣬��Na2SO3���л�ԭ�ԣ���H2O2����������ԭ��Ӧ����������������������ؾ���ǿ�����ԣ���H2O2����������ԭ��Ӧ��Ҳ������������
�ʴ�Ϊ��ab��
��6��M�ǽ����ǽ������Σ�����Mһ������Σ�Z��N���ĵ��ʣ���ΪAl���ƶ�N����������Z���������������ݲ����Ϸ�Ӧ��X+Y+H2O��Al��OH��3+NH4+ ��֪���÷�ӦΪ���κ�һˮ�ϰ��ķ�Ӧ����X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ��Al3++3NH3+3H2O=Al��OH��3��+3NH4+��N���ĵ��ʵĻ�ѧ����ʽΪ��2Al2O3�����ڣ�$\frac{\underline{\;\;\;���\;\;\;}}{����ʯ}$ 4Al+3O2����
�ʴ�Ϊ��Al3++3NH3+3H2O=Al��OH��3��+3NH4+��2Al2O3�����ڣ�$\frac{\underline{\;\;\;���\;\;\;}}{����ʯ}$ 4Al+3O2����
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɡ�Ԫ�ػ������ƶϵȣ����ض�Ԫ���������뻯ѧ����Ŀ��飬ע���Ԫ�����ڱ���������գ��Ѷ��еȣ�

| A�� | ��������ֵ�Ԫ���У�����Ԫ�غͷǽ���Ԫ��������� | |
| B�� | Ԫ�����ڱ���18������16���壬��Ϊ���塢���塢�ڢ�������� | |
| C�� | Ԫ�����ڱ����߸����ڣ���Ϊ�����ںͳ����ںͲ���ȫ���� | |
| D�� | ���������ڱ��н�����ǽ����ķֽ紦�����ҵ��뵼����ϣ���衢��� |
| A�� | PCl5�����Ƿ��Ӿ��� | |
| B�� | PCl5���������õĵ����� | |
| C�� | PCl5������[PCl4]+��[PCl6]-���ɣ���������Ŀ֮��Ϊ1��1 | |
| D�� | PCl5������[PCl3]2+��[PCl7]2-���ɣ���������Ŀ֮��Ϊ1��1 |
| A�� | 14g��ϩ�ͱ�ϩ�Ļ�������к���Hԭ����Ϊ2NA | |
| B�� | ��״����2.24L�Ҵ�������Na��Ӧ����H2������0.05NA | |
| C�� | ÿĦ��-CH3�к�10NA������ | |
| D�� | ÿĦ���ױ��к��е�̼̼��������ĿΪ7 NA |
| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
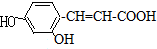 ��
��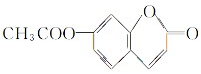 ��
��