题目内容
化学实验是科学探究的基础.请回答有关实验问题:
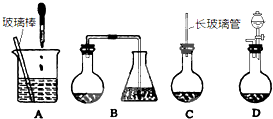
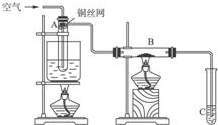
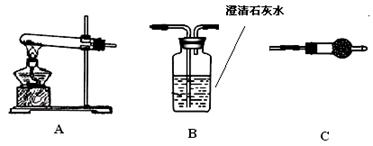
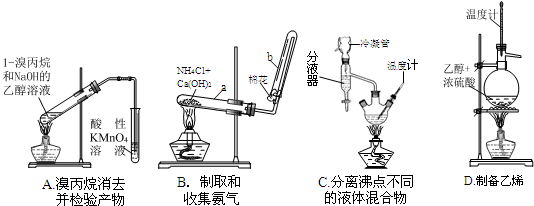
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是______:
(2)要检验上面B装置氨气已集满的操作是______则试管已集满.
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如表:
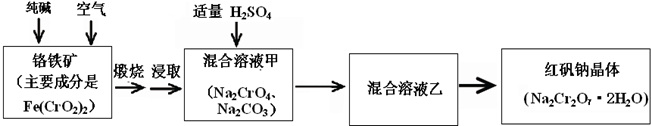
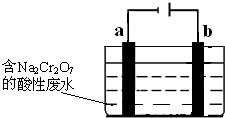
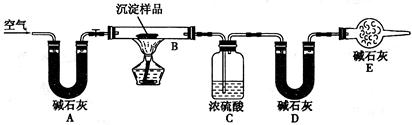
①由表可以看出:保存液态ClO2的条件是密封、______;ClO2与碱反应的离子方程式为______;观察“图A”,要从NaClO2溶液制得不含结晶水的晶体,操作是蒸发结晶,控制条件是______;应控制析出晶体的温度范围是______.
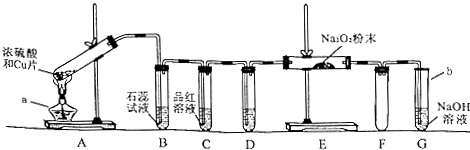
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用图B所示装置模拟工业制法制取并收集液态ClO2,请模仿图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注.

(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是______:

(2)要检验上面B装置氨气已集满的操作是______则试管已集满.
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如表:
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃ 红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用图B所示装置模拟工业制法制取并收集液态ClO2,请模仿图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注.

(1)A.加热挥发出的乙醇被酸性高锰酸钾氧化,所以乙醇也能时酸性高锰酸钾溶液褪色,从而导致干扰烯烃的检验,故A错误;
B.实验室用氯化铵和氢氧化钙加热制取氨气,氨气易溶于水,和氧气在常温下不反应,密度小于空气,所以氨气采用向下排空气法收集,故B正确;
C.蒸馏分离混合物时,温度计测量馏分温度而不是混合溶液温度,故C错误;
D.乙醇和浓硫酸在170℃条件下制取乙烯,温度计测量混合溶液温度,故D错误;
故选B;
(2)氨气能使湿润的红色石蕊试纸变蓝色,氨气和氯化氢反应产生白烟,所以可以用浓盐酸或湿润的红色石蕊试纸检验氨气,其检验方法为:取用水湿润的pH试纸(或红色石蕊试纸,或粘有浓氨水的玻棒)靠近b管口,若试纸变红,故答案为:取用水湿润的pH试纸(或红色石蕊试纸,或粘有浓氨水的玻棒)靠近b管口,若试纸变红;
(3)①二氧化氯的熔点较低,易挥发,所以二氧化氯要密封且低温避光保存;
二氧化氯和碱反应生成亚氯酸盐和氯酸盐,同时还生成水,离子反应方程式为2ClO2+2OH-═ClO2-+ClO3-+H2O;
从溶解度曲线可以看出,常压在略高于38℃时蒸发留在母液中的NaClO2太多,只有减压时蒸发,在略高于38℃时水分挥发多一些、母液少一些;
根据图象知,当温度略高于38℃时析出氯酸钠晶体,所以蒸发结晶析出氯酸钠晶体时,温度控制在略高于(或大于)38℃,
故答案为:低温避光;2ClO2+2OH-═ClO2-+ClO3-+H2O;减压蒸发;略高于(或大于)38℃;
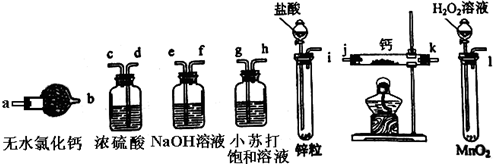
②潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,所以要用温度计控制混合溶液温度,二氧化氯常温下是气体,其熔点较低,要使其变为液体,应该采用冰水混合物冷却,二氧化氯有毒不能直接排空,所以要有尾气处理装置,所以该装置图为 ,
,
故答案为: .
.
B.实验室用氯化铵和氢氧化钙加热制取氨气,氨气易溶于水,和氧气在常温下不反应,密度小于空气,所以氨气采用向下排空气法收集,故B正确;
C.蒸馏分离混合物时,温度计测量馏分温度而不是混合溶液温度,故C错误;
D.乙醇和浓硫酸在170℃条件下制取乙烯,温度计测量混合溶液温度,故D错误;
故选B;
(2)氨气能使湿润的红色石蕊试纸变蓝色,氨气和氯化氢反应产生白烟,所以可以用浓盐酸或湿润的红色石蕊试纸检验氨气,其检验方法为:取用水湿润的pH试纸(或红色石蕊试纸,或粘有浓氨水的玻棒)靠近b管口,若试纸变红,故答案为:取用水湿润的pH试纸(或红色石蕊试纸,或粘有浓氨水的玻棒)靠近b管口,若试纸变红;
(3)①二氧化氯的熔点较低,易挥发,所以二氧化氯要密封且低温避光保存;
二氧化氯和碱反应生成亚氯酸盐和氯酸盐,同时还生成水,离子反应方程式为2ClO2+2OH-═ClO2-+ClO3-+H2O;
从溶解度曲线可以看出,常压在略高于38℃时蒸发留在母液中的NaClO2太多,只有减压时蒸发,在略高于38℃时水分挥发多一些、母液少一些;
根据图象知,当温度略高于38℃时析出氯酸钠晶体,所以蒸发结晶析出氯酸钠晶体时,温度控制在略高于(或大于)38℃,
故答案为:低温避光;2ClO2+2OH-═ClO2-+ClO3-+H2O;减压蒸发;略高于(或大于)38℃;
②潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,所以要用温度计控制混合溶液温度,二氧化氯常温下是气体,其熔点较低,要使其变为液体,应该采用冰水混合物冷却,二氧化氯有毒不能直接排空,所以要有尾气处理装置,所以该装置图为
 ,
,故答案为:
 .
.
练习册系列答案
相关题目
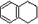 ,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下: