题目内容
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
I.(1)已知:一定条件下![]() 可被甲烷还原“纳米级”的金属铁。其反应为:
可被甲烷还原“纳米级”的金属铁。其反应为:
![]()
①此反应的化学平衡常数表达式为______
②在容积均为VL的I、II、III三个相同密闭容器中加入足量![]() ,然后分别充入amol
,然后分别充入amol![]() ,三个容器的反应温度分别为
,三个容器的反应温度分别为![]() 、
、![]() 、
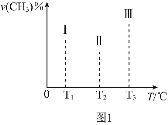
、![]() 且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时
且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时![]() 的体积分数如图1所示,此时I、II、III三个容器中一定处于化学平衡状态的是______;上述反应的
的体积分数如图1所示,此时I、II、III三个容器中一定处于化学平衡状态的是______;上述反应的![]() ______
______![]() 填“大于”或“小于”
填“大于”或“小于”![]() ,该反应在______
,该反应在______![]() 填“高温”、“低温”或“任意温度”
填“高温”、“低温”或“任意温度”![]() 下可自发进行。
下可自发进行。
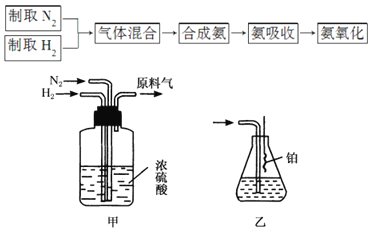
![]() 利用天然气为原料的一种工业合成氨简式流程图如图2:
利用天然气为原料的一种工业合成氨简式流程图如图2:
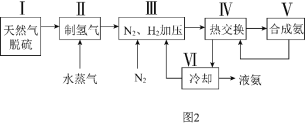
(1)步骤Ⅱ中制氢气的原理如下:Ⅰ![]() ;
;![]()
Ⅱ![]() ;
;![]()
①对于反应Ⅰ,在一定温度下的恒容容器中,表示其已达到最大化学反应限度的叙述正确的是______。
A.单位时间内1mol![]() 消耗,同时有3mol
消耗,同时有3mol![]() 生成;
生成;
B.![]() 、
、![]() 、CO的物质的量浓度相等;
、CO的物质的量浓度相等;
C.混合气体的密度再改变;
D.混合气体的压强不再改变。
②则反应![]() ;
;![]() ______
______![]() 用含
用含![]() 、
、![]() 的代数式表示
的代数式表示![]() 。
。
(2)合成氨是人类科学技术上的一项重大突破,反应原理为:![]() 在容积为10L的密闭容器中进行,起始时充入
在容积为10L的密闭容器中进行,起始时充入![]()
![]() 、
、![]()
![]() 反应在不同条件下进行,反应体系总压强随时间的变化如图3所示。
反应在不同条件下进行,反应体系总压强随时间的变化如图3所示。
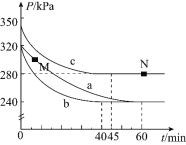
①实验a从开始至平衡时的反应速率![]() ______;实验c中
______;实验c中![]() 的平衡转化率
的平衡转化率![]() 为______。
为______。
②与实验a相比,其他两组改变的实验条件是:b______,c______。
③M点的逆反应速率![]() ______N点的正反应速率
______N点的正反应速率![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;N点时再加入一定量
;N点时再加入一定量![]() ,平衡后
,平衡后![]() 的体积分数______
的体积分数______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() 。
。
【答案】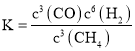 Ⅲ 大于 高温 D
Ⅲ 大于 高温 D ![]()
![]()
![]() 使用催化剂 增大压强
使用催化剂 增大压强 ![]() 增大
增大
【解析】
Ⅰ固相和气相均存在的反应,固相的浓度项不列入化学平衡常数表达式;根据图中Ⅰ、Ⅱ、Ⅲ图象,![]() 百分含量随温度的变化解答;根据温度对平衡的影响来判断,升高温度平衡正向移动,
百分含量随温度的变化解答;根据温度对平衡的影响来判断,升高温度平衡正向移动,![]() 的含量增大,据此判断
的含量增大,据此判断![]() 大小,再由焓变和熵变判断反应自发进行的条件;
大小,再由焓变和熵变判断反应自发进行的条件;
Ⅱ在一定条件下,反应I达到最大反应限度时,说明反应达到化学平衡,各组分浓度不再改变,体系压强不再改变,正逆反应速率相等,据此逐项分析;根据反应Ⅰ和反应Ⅱ推导所求反应,由多重平衡规则计算该反应的化学平衡常数;
![]() 根据
根据![]() 计算
计算![]() 的消耗速率,根据转化率
的消耗速率,根据转化率![]() 计算
计算![]() 的平衡转化率
的平衡转化率![]() ;与实验a相比,实验b和实验a的平衡状态一致,实验b比实验a提前到达化学平衡,实验c的压强大于实验a的压强;实验c的压强大于实验a的压强,增大压强有利于增大化学反应速率,N点达到化学平衡状态,再加入一定量
;与实验a相比,实验b和实验a的平衡状态一致,实验b比实验a提前到达化学平衡,实验c的压强大于实验a的压强;实验c的压强大于实验a的压强,增大压强有利于增大化学反应速率,N点达到化学平衡状态,再加入一定量![]() ,促使化学平衡正向移动。
,促使化学平衡正向移动。
Ⅰ(1) ①固相和气相均存在的反应,固相的浓度项不列入化学平衡常数表达式,该反应的化学平衡常数表达式为: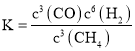 ;
;
故答案为: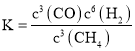 ;
;
![]() 在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”的金属铁,然后分别充入
在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”的金属铁,然后分别充入![]() ,
,![]() ,根据图中Ⅰ、Ⅱ、Ⅲ图象,温度逐渐升高,三个容器中的
,根据图中Ⅰ、Ⅱ、Ⅲ图象,温度逐渐升高,三个容器中的![]() 百分含量没有呈整体上升的趋势,则其中肯定有一个达到了平衡,温度升高,反应速率加快,可知先达到平衡的是容器III前两个容器没有达到平衡,且随温度升高,
百分含量没有呈整体上升的趋势,则其中肯定有一个达到了平衡,温度升高,反应速率加快,可知先达到平衡的是容器III前两个容器没有达到平衡,且随温度升高,![]() 百分含量下降,可知升高温度平衡正向进行,反应
百分含量下降,可知升高温度平衡正向进行,反应![]() 的
的![]() 大于0,反应气体分子数增多,熵增,即
大于0,反应气体分子数增多,熵增,即![]() ,反应放热,
,反应放热,![]() ,所以反应在高温下自发;
,所以反应在高温下自发;
故答案为:Ⅲ;大于;高温;
Ⅱ(1) ①单位时间内1mol![]() 消耗,必然同时有3mol
消耗,必然同时有3mol![]() 生成,说明反应正向进行,并不能说明反应已经达到化学平衡,故A错误;
生成,说明反应正向进行,并不能说明反应已经达到化学平衡,故A错误;![]() 、
、![]() 、CO的物质的量浓度关系取决于反应物的充入量以及反应进行的程度,并不能通过三者物质的量浓度相等说明反应达到化学平衡,故B错误;混合气体的密度为
、CO的物质的量浓度关系取决于反应物的充入量以及反应进行的程度,并不能通过三者物质的量浓度相等说明反应达到化学平衡,故B错误;混合气体的密度为![]() ,反应前后质量守恒,m不变,反应在恒容容器中进行,V不变,则整个过程混合气体密度
,反应前后质量守恒,m不变,反应在恒容容器中进行,V不变,则整个过程混合气体密度![]() 不变,无法判断化学反应是否达到化学平衡,故C错误;反应前后气体分子数改变,体系压强发生变化,可以通过压强判断化学反应是否达到平衡,故D正确;
不变,无法判断化学反应是否达到化学平衡,故C错误;反应前后气体分子数改变,体系压强发生变化,可以通过压强判断化学反应是否达到平衡,故D正确;
故答案为:D;
![]() 所求反应可由Ⅰ
所求反应可由Ⅰ![]() Ⅱ得到,根据多重平衡规则,所求反应的化学平衡常数为
Ⅱ得到,根据多重平衡规则,所求反应的化学平衡常数为![]() ;
;
故答案为:![]() ;
;
![]() 实验a中,起始时体系压强为320kPa,平衡时体系压强为240kPa,
实验a中,起始时体系压强为320kPa,平衡时体系压强为240kPa,
![]()
起始![]()
![]() 0
0
转化![]() x3x 2x
x3x 2x
平衡![]()
![]() 2x
2x
则有![]() ,可得
,可得![]() ,
,
所以实验a从开始至平衡时的反应速率![]() ,
,
实验中![]() 的平衡转化率
的平衡转化率![]() 为
为![]() ;
;
故答案为:![]() ;
;![]() ;
;
![]() 与实验a相比,实验b和实验a的平衡状态一致,实验b比实验a提前到达化学平衡,由此可判断实验b改变的条件是使用催化剂,
与实验a相比,实验b和实验a的平衡状态一致,实验b比实验a提前到达化学平衡,由此可判断实验b改变的条件是使用催化剂,
实验c的压强大于实验a的压强,由此可判断实验c改变的条件是增大压强;
故答案为:使用催化剂;增大压强;
![]() 实验c的压强大于实验a的压强,增大压强有利于增大化学反应速率,所以M点的逆反应速率
实验c的压强大于实验a的压强,增大压强有利于增大化学反应速率,所以M点的逆反应速率![]() 点的正反应速率
点的正反应速率![]() ;N点达到化学平衡状态,再加入一定量
;N点达到化学平衡状态,再加入一定量![]() ,促使化学平衡正向移动,则平衡后
,促使化学平衡正向移动,则平衡后![]() 的体积分数增大;
的体积分数增大;
故答案为:![]() ;增大。
;增大。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应生成一种无氧酸和两种氮的常见氧化物。亚硝酰氯应用广泛,可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组同学拟制备原料气NO和Cl2,制备装置如图所示,为制备纯净干燥的气体,补充右表中缺少的药品。
装置Ⅰ | 装置Ⅱ | ||
蒸馏烧瓶中 | A仪器中 | ||
制备纯净的Cl2 | MnO2 | ①______ | ②______ |
制备纯净的NO | Cu | ③______ | ④______ |
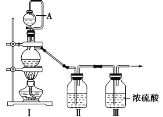
(2)乙组同学对甲组同学制取NO的装置略加改良,结合甲组制得的Cl2共同制备NOCl,装置如图所示:
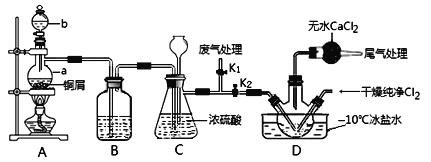
①仪器b的名称为________________。
②组装好实验装置后应先______________,然后依次装入药品。此实验关键操作有两点:一是将Cl2充满D装置的三颈瓶中;二是A中反应开始时要先关闭K2,打开K1,待NO充满装置后再关闭K1,打开K2。这两步操作中充满的目的都是__________________________________________________。
③若C装置中压强过大,可以观察到的现象是_________________________。
④装置D中冰盐水的作用是__________________。
(3)亚硝酰氯(NOCl)纯度的测定:将所得亚硝酰氯(NOCl)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用0.8mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)与水反应的化学方程式为_________________________。
②亚硝酰氯(NOCl)的质量分数为______________________。
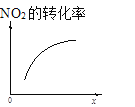
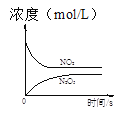
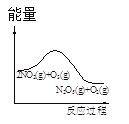
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
A | B | C | D |
|
|
|
|
t1时仅加入催化剂,平衡向正方向移动 | 达平衡时,仅改变x,则x为c(O2) | 从反应开始达平衡气体浓度变化 | 升高温度,平衡常数减小 |
A.AB.BC.CD.D
【题目】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
t∕min | 2 | 4 | 7 | 9 |
n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前4min的平均反应速率υ(Z)=0.0125molL-1min-1
B. 其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正)
C. 其他条件不变,再充入0.2molZ,达平衡时X的体积分数增大
D. 该温度下此反应的平衡常数K=1.44
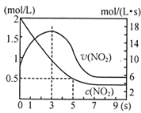
【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。