题目内容
【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。
【答案】2.5×103 = 2.8 0.10 60% 57.5 g·mol1 减小 向左移动
【解析】
(1)根据方程式可知,20s时二氧化氮的变化量△n=0.05mol×2=0.1mol,根据![]() 计算二氧化氮表示的平均反应速率;
计算二氧化氮表示的平均反应速率;
(2)根据表格中数据知,60s、80s时四氧化二氮的物质的量均为0.08mol,则反应达到平衡状态;平衡时,则二氧化氮的物质的量为0.40mol-0.08mol×2=0.24mol,四氧化二氮、二氧化氮的浓度分别为0.04mol·L-1、0.12mol·L-1,进而计算平衡常数;
(3)若在相同条件下最初向该容器中充入四氧化二氮气体,要达到上述平衡状态,则该平衡状态与原平衡状态为完全等效平衡,则四氧化二氮的起始物质的量应该是0.20mol;
(4)该平衡状态与原平衡状态为完全等效平衡,平衡时,四氧化二氮的物质的量为0.08mol,二氧化氮的物质的量为0.24mol;
(5)升高温度,气体颜色会变深,说明升高温度平衡逆向移动,则平衡常数的值将减小;
(6)He是惰性气体,不参与反应,但容器体积扩大,压强减小,平衡将向气体体积减小的方向移动。
(1)根据方程式可知,20s时二氧化氮的变化量△n=0.05mol×2=0.1mol,用二氧化氮表示的平均反应速率为![]() ;
;
故答案为:2.5×103;
(2)根据表格中数据知,60s、80s时四氧化二氮的物质的量均为0.08mol,则反应达到平衡状态,则二氧化氮的物质的量也保持不变,n3=n4;平衡时,则二氧化氮的物质的量为0.40mol-0.08mol×2=0.24mol,四氧化二氮、二氧化氮的浓度分别为0.04mol·L-1、0.12mol·L-1,故平衡常数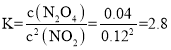 ;
;
故答案为:=;2.8;
(3)若在相同条件下最初向该容器中充入四氧化二氮气体,要达到上述平衡状态,则该平衡状态与原平衡状态为完全等效平衡,则四氧化二氮的起始物质的量应该是0.20mol,其![]() ;
;
故答案为:0.10;
(4)该平衡状态与原平衡状态为完全等效平衡,平衡时,四氧化二氮的物质的量为0.08mol,二氧化氮的物质的量为0.24mol,故转化率![]() ;混合气体的总物质的量为(0.80+0.24)mol=0.32mol,平均摩尔质量为
;混合气体的总物质的量为(0.80+0.24)mol=0.32mol,平均摩尔质量为![]() ;
;
故答案为:60%;57.5 g·mol1;
(5)升高温度,气体颜色会变深,说明升高温度平衡逆向移动,则平衡常数的值将减小;
故答案为:减小;
(6)He是惰性气体,不参与反应,但容器体积扩大,压强减小,平衡将向气体体积减小的方向移动,即向左移动;
故答案为:向左移动。