题目内容
【题目】短周期元素X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的核外p电子数比s电子数少1个,Z的一种超原子![]() 具有40个价电子,下列说法错误的是( )
具有40个价电子,下列说法错误的是( )
A.![]() 的空间构型为平面三角形
的空间构型为平面三角形
B.简单离子半径:![]()
C.![]() 中心原子的杂化方式为
中心原子的杂化方式为![]() 杂化
杂化
D.化合物ZY的结构与X的某种单质的结构相似
【答案】B
【解析】
X、Y、Z是原子序数依次增大的短周期元素,Z的一种超原子![]() 具有40个价电子,则Z的价电子数为
具有40个价电子,则Z的价电子数为![]() 个,Z为Al元素,Y元素基态原子的核外p电子数比s电子数少1个,Y为N元素,X元素基态原子有2个未成对电子,X为C元素,据此分析解答。
个,Z为Al元素,Y元素基态原子的核外p电子数比s电子数少1个,Y为N元素,X元素基态原子有2个未成对电子,X为C元素,据此分析解答。
A.CO32-的中心原子的价电子对数为![]() ,不含孤电子对,采用sp2杂化,空间构型为平面三角形,A选项正确;
,不含孤电子对,采用sp2杂化,空间构型为平面三角形,A选项正确;
B.N3-与Al3+的核外电子层数相同,而N的核电荷数小于Al,则离子半径:N3->Al3+,B选项错误;
C.NO3-的中心原子的价电子对数为![]() ,不含孤电子对,采用sp2杂化,C选项正确;
,不含孤电子对,采用sp2杂化,C选项正确;
D.化合物ZY为AlN,是原子晶体,属于类金刚石氮化物,与C的单质金刚石结构相似,D选项正确;
答案选B。

 优加精卷系列答案
优加精卷系列答案【题目】(1)已知常温时,0.1mol/L醋酸在水中有0.1%发生电离,则该溶液的pH=_____,醋酸的电离平衡常数Ka=______。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示:
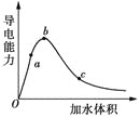
①a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是___。
②a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)_______c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
(3)25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | NH3·H2O | H2CO3 | HCN |
电离平衡常数 | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=5.0×10-10 |
请回答下列问题:
①H2CO3的第二级电离平衡常数的表达式Ka2=_______。
②25℃时,向0.1molL-1的氨水中缓缓通入CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是___。
A.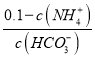 B.
B.![]() C.
C.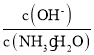 D.
D.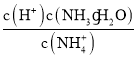
③向NaCN溶液中通入少量CO2气体,发生反应的离子方程式为___。