题目内容
【题目】一定温度下,冰醋酸加水稀释过程中溶液的导电能力实验结果如图所示:
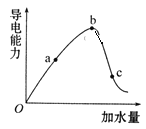
(1)“O”点为什么不导电?____________。
(2)比较a、b、c三点的c(H+)大小。____________(用“﹥”“=” 或“﹤”)
(3)a、b、c三点中,醋酸的电离程度最大的是哪一点?____________。
(4)若要使c点溶液中的c(CH3COO-)增大,试列举两条可行的措施______。
(5)在稀释过程中,c(H+)、n(H+)、c(OH-)和n(CH3COOH)中,始终保持增大趋势的是_________。
【答案】冰醋酸还没有电离 b>a>c c 加热 ,加CH3COONa固体(或其它合理答案 n(H+),c(OH-)
【解析】
从图中可以看出,从0点到b点,溶液的导电能力增强,说明溶液中离子浓度增大;从b点到c点,溶液的导电能力减弱,说明溶液中离子浓度减小。
(1)在“O”点,只有冰醋酸,冰醋酸不发生电离,不存在自由离子,所以不导电。
答案为:冰醋酸还没有电离
(2从导电能力看,导电能力b>a>c,则溶液中c(H+)关系为b>a>c。答案为:b>a>c
(3)从a点到b点,再到c点,醋酸中不断加水,醋酸不断稀释,浓度不断减小,所以电离程度不断增大,电离程度最大的是c点。答案为:c
(4)若要使c点溶液中的c(CH3COO-)增大,可采取的措施是加热、加CH3COONa固体,也可加入冰醋酸。
答案为:加热、加CH3COONa固体等。
(5)在稀释过程中,n(H+)、c(OH-)增大,c(H+)、n(CH3COOH)减小,始终保持增大趋势的是n(H+)、c(OH-)。答案为:n(H+)、c(OH-)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目