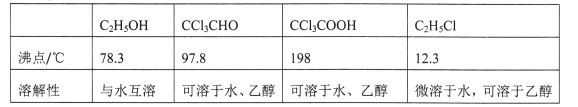
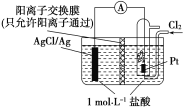
��Ŀ����
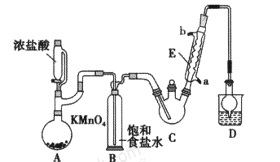
����Ŀ�����������Һ��Ӧ���ڵ��¡�ϡ����Һ����Ҫ������ClO-��Cl-����75�����ϡ�Ũ����Һ����Ҫ������ClO3-��Cl-���о�С��������ʵ��װ����ȡ�����(KClO3)�����ⶨ�䴿�ȡ�

aΪŨ���ᣬbΪMnO2��cΪ����ʳ��ˮ��dΪ30%KOH��Һ��eΪNaOH��Һ
�ش���������:
��1�����װ�������Ժ�����ҩƷ����װ��IIIˮ������75�濪ʼ��Ӧ��
��װ��I�з�Ӧ�����ӷ���ʽΪ_______________��
����ȡ��װ��II���Ա�ʵ���Ӱ����_______________��
��ʵ����������װ��IǰΪ�˷�ֹ���������ݳ����ɲ�ȡ�Ĵ�ʩ��_______________��
�ܴ�װ��III���Թ��з���õ�KClO3�ֲ�Ʒ�����л��е�������KClO��______________��
��2��Ϊ�ⶨ��ƷKClO3�Ĵ��ȣ���������ʵ��:
����1:ȡ2.45g��Ʒ����ˮ���250mL��Һ��
����2:ȡ25.00mL��Һ����ƿ�У�����pH=10���μ�����H2O2��Һ������Գ���ClO-��Ȼ�������Һ1��2���ӣ���ȴ��
����3:�������KI��Һ������μ�������ϡ���ᡣ(ClO3-+6I-+6H+=Cl-+3I2+3H2O)
����4:����ָʾ������0.5000mol/LNa2S2O3����Һ�ζ����յ㣬���ı���Һ20.00mL�� (2S2O32-+I2=S4O62-+2I-)
�ٲ���2�г�ȥC1O-�����ӷ���ʽ��_____________������С���Ŀ����_________��
�ڱȽϼ���������������ClO3-_______C1O-(��д��>����<��)��
����Ʒ��KClO3��ؠ������Ϊ________��(�𰸱�����λ��Ч����,KClO3ʽ��:122.5)
���𰸡�MnO2+4H++2Cl����Ũ��![]() Mn2++ Cl2��+2H2O ���� HCl ���������������أ�ʹ KClO3 ���ʽ��� ��װ�â��е���Һ�ӷ�Һ©����ע��Բ����ƿ KCl ClO��+H2O2
Mn2++ Cl2��+2H2O ���� HCl ���������������أ�ʹ KClO3 ���ʽ��� ��װ�â��е���Һ�ӷ�Һ©����ע��Բ����ƿ KCl ClO��+H2O2 ![]() O2��+Cl��+H2O(���� OH��) ʹ������ H2O2�ֽ⣬��ֹ������ KI < 83.3%
O2��+Cl��+H2O(���� OH��) ʹ������ H2O2�ֽ⣬��ֹ������ KI < 83.3%
��������
��1����װ��I�ж���������Ũ���ᷴӦ�����Ȼ�����������ˮ����װ��II��Ϊ����ʳ��ˮ�����Գ�ȥ�����е��Ȼ�������������������Һ����װ��I�е������������������Һ��Ӧ���ڵ��¡�ϡ����Һ����Ҫ������ClO-��Cl-����75�����ϡ�Ũ����Һ����Ҫ������ClO3-��Cl-����2���ٲ���2���ڼ���������ClO����H2O2��ԭΪCl����������п���ʹ������ H2O2�ֽ����ڸ���������������������ClO��������H2O2��ClO3-��������H2O2��������ClO3-+6I-+6H+=Cl-+3I2+3H2O��2S2O32-+I2=S4O62-+2I-���ɵ÷�Ӧ�Ĺ�ϵʽClO3------6S2O32-�����ù�ϵʽ������Ʒ��KClO3��ؠ��������
��1����װ��I�ж���������Ũ���ᷴӦ�����Ȼ�����������ˮ����Ӧ���ӷ���ʽ��MnO2+4H++2Cl����Ũ��![]() Mn2++ Cl2��+2H2O����װ��II��Ϊ����ʳ��ˮ�����Գ�ȥ�����е��Ȼ�������ȡ��װ��II������ HCl ���������������أ�ʹ KClO3 ���ʽ�������ʵ����������װ��IǰΪ�˷�ֹ���������ݳ����ɲ�ȡ�Ĵ�ʩ�ǽ�װ�â��е�����������Һ�ӷ�Һ©����ע��Բ����ƿ�������������Һ��Ӧ���ڵ��¡�ϡ����Һ����Ҫ������ClO-��Cl-����75�����ϡ�Ũ����Һ����Ҫ������ClO3-��Cl-�����Դ�װ��III���Թ��з���õ�KClO3�ֲ�Ʒ�����л��е�������KClO��KCl�� ��2���ٲ���2���ڼ���������ClO����H2O2��ԭΪCl������Ӧ�����ӷ���ʽ��ClO��+H2O2
Mn2++ Cl2��+2H2O����װ��II��Ϊ����ʳ��ˮ�����Գ�ȥ�����е��Ȼ�������ȡ��װ��II������ HCl ���������������أ�ʹ KClO3 ���ʽ�������ʵ����������װ��IǰΪ�˷�ֹ���������ݳ����ɲ�ȡ�Ĵ�ʩ�ǽ�װ�â��е�����������Һ�ӷ�Һ©����ע��Բ����ƿ�������������Һ��Ӧ���ڵ��¡�ϡ����Һ����Ҫ������ClO-��Cl-����75�����ϡ�Ũ����Һ����Ҫ������ClO3-��Cl-�����Դ�װ��III���Թ��з���õ�KClO3�ֲ�Ʒ�����л��е�������KClO��KCl�� ��2���ٲ���2���ڼ���������ClO����H2O2��ԭΪCl������Ӧ�����ӷ���ʽ��ClO��+H2O2![]() O2��+Cl��+H2O��������п���ʹ������H2O2�ֽ�������С���Ŀ����ʹ������ H2O2�ֽ⣬��ֹ������ KI���ڸ���������������������ClO��������H2O2��ClO3-��������H2O2������������ClO3-<C1O-������25.00mL��Һ�к���KClO3��ؠ��Ϊxg��
O2��+Cl��+H2O��������п���ʹ������H2O2�ֽ�������С���Ŀ����ʹ������ H2O2�ֽ⣬��ֹ������ KI���ڸ���������������������ClO��������H2O2��ClO3-��������H2O2������������ClO3-<C1O-������25.00mL��Һ�к���KClO3��ؠ��Ϊxg��
KClO3-----6S2O32-
122.5g 6mol
xg 0.5mol/L![]() 0.02L
0.02L
![]()
x=0.204g
��Ʒ��KClO3��ؠ������Ϊ![]() 83.3% ��
83.3% ��