题目内容
【题目】某超市中一种电池外壳的纸层包装上印有如图所示的文字,根据要求回答:
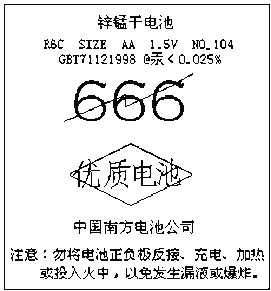
(1)该电池的种类是______(填序号).
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中,毒性最大的是______(写元素符号).
(3)该电池的使用和性能,下列说法中不正确的是______
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境
(4)已知该电池的总反应为:Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,写出该电池放电时的正负极反应方程式:
负极___________________________________
正极___________________________________
【答案】 ① 汞 B C Zn – 2e = Zn2+ 2MnO2+ 2e +2NH4+=2NH3↑+Mn2O3+H2O
【解析】试题分析:由图中信息可知,该电池为锌锰干电池,不可充电或投入火中。其中汞含量小于0.025%,由于汞可以严重污染环境,故该电池不可随意丢弃,用后应回收处理。
(1)该电池的种类是干电池,填①.
(2)该电池含有的金属元素中,毒性最大的是汞.
(3)A.该电池可应用于闹钟、收音机、照相机等,A正确;B.该电池不可充电,是一次电池,B不正确; C.该电池使用后不能投入火中,不能埋入地下以防污染环境,C不正确。综上所述,关于该电池的使用和性能,以上说法中不正确的是B C。
(4)该电池的总反应为Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O,由总反应可知,Zn是负极,其发生氧化反应,其电极反应式为Zn – 2e = Zn2+,由总反应式和负极反应式可以写出正极的电极反应式为2MnO2+ 2e +2NH4+=2NH3↑+Mn2O3+H2O。

【题目】下列为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
关于已知元素C、N、S和未知的元素X、Y、Z,回答下列问题:
(1)Z元素在周期表中的位置为______________。
(2)表中元素原子半径最大的是______________ (写元素符号)。
(3)①S与Z可形成化合物S2Z2,写出它的电子式______________。
②C、N、S三元素形成的阴离子常用于检验Fe3+的存在,写出它的结构式______________。
(4)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体A、B均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为______________,生成硫酸铜物质的量为______________。

