题目内容
【题目】原子序数依次增大的a、b、c、d四种主族元素,其中a和d同族,a-的电子层结构与氦相同,b和c的次外层有8个电子,b2-、c-和d+的电子层结构相同。下列错误的是( )
A.元素的非金属性次序为c>b>a
B.b2-的还原性弱于c-的还原性
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
【答案】B
【解析】
![]() 的电子层结构与氦相同,则a为氢,d与a同族,因此d也位于第IA族,结合b、c来考虑,d为钾,则b为硫,c为氯,据此来分析各选项即可。
的电子层结构与氦相同,则a为氢,d与a同族,因此d也位于第IA族,结合b、c来考虑,d为钾,则b为硫,c为氯,据此来分析各选项即可。
A.根据元素周期律,越右上角的元素,其非金属性越强,因此非金属性为氯>硫>氢,即![]() ,A项正确;
,A项正确;
B.单质的氧化性越强,其对应的简单离子的还原性越弱,![]() 的氧化性强于
的氧化性强于![]() ,因此
,因此![]() 的还原性弱于
的还原性弱于![]() ,B项错误;
,B项错误;
C.d与其它3种元素可以形成![]() 、
、![]() 和
和![]() 三种离子化合物,C项正确;
三种离子化合物,C项正确;
D.氢元素的最高价为+1,最低价为-1,代数和为0;硫元素的最高价为+6,最低价为-2,代数和为4;氯元素的最高价为+7,最低价为-1,代数和为6,D项正确;
答案选B。

【题目】实验室用50mL0.50mol·L-1盐酸、50mL0.50mol·L-1NaOH溶液和如图所示装置进行测定中和热的实验,得到表中的数据:
实验次数 | 起始温度 | 终止温度 | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
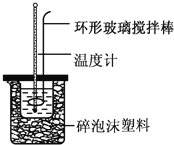
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是_______
(2)根据上表中所测数据进行计算,则该实验测得的中和热△H=__________(盐酸和NaOH溶液的密度按1gcm-3计算,反应后混合溶液的比热容C按4.18J(g℃)-1计算,结果保留小数点后一位)。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,则实验中测得的“中和热”为△H1,则△H1与△H的关系为△H1________△H(填“大于”、“小于”、“等于”)。如改用60mL0.5mol·L-1的盐酸与50mL 0.55mol·L-1的NaOH 溶液进行反应,与上述实验相比,所放出的热量_______(填“相等”或“不相等”),所求中和热___(填“相等”或“不相等”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是___(填字母序号)。
A 测量盐酸的温度后,温度计没有用水冲洗干净
B 把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C 做本实验的当天室温较高
D 将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E 在量取盐酸时仰视计数
F 大烧杯的盖板中间小孔太大.
【题目】碳是构成物质世界最重要的元素之一,能形成众多的化合物。
![]() 已知
已知![]() 碳完全燃烧可放出3148kJ热量,
碳完全燃烧可放出3148kJ热量,![]() 液态水汽化时要吸收44kJ热量。
液态水汽化时要吸收44kJ热量。
![]()
![]()
![]()
![]()
请写出制备水煤气的热化学方程式________。
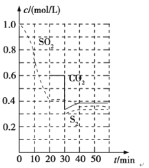
![]() 恒容密闭容器中发生
恒容密闭容器中发生![]() 反应,当通入不同量的
反应,当通入不同量的![]() 和
和![]() 充分反应后得到如下实验数据:
充分反应后得到如下实验数据:
实验组 | 温度
| 起始量
| 平衡量
| 达到平衡所需的时间 | ||
|
|
|
| |||
1 | 650 | 2 |
|
| 2 | 4 |
2 | 650 |
|
|
|
| 5 |
![]() 由实验组1数据可知,达到平衡时
由实验组1数据可知,达到平衡时![]() ________mol/(Lmin)。
________mol/(Lmin)。
![]() 由实验组1和2数据分析可知,增大压强对该可逆反应的影响是________。
由实验组1和2数据分析可知,增大压强对该可逆反应的影响是________。
![]() 若在一定温度、容积可变的密闭容器中发生上述反应,下列说法中可判断该反应达到平衡状态的是________。
若在一定温度、容积可变的密闭容器中发生上述反应,下列说法中可判断该反应达到平衡状态的是________。![]() 填编号
填编号![]()
a.容器中压强不变 b.1molH-H键断裂,同时断裂2molO-H键
c.c(H2O)=c(CO) d.v(H2O)=v(H2) e..容器体积不变
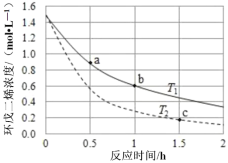
![]() 取
取![]() 草酸亚铁晶体(FeC2O4)样品在惰性气体保护气下加热,测得加热过程中样品质量随温度变化的曲线如图所示:
草酸亚铁晶体(FeC2O4)样品在惰性气体保护气下加热,测得加热过程中样品质量随温度变化的曲线如图所示:
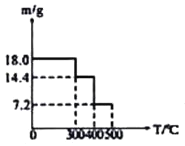
350℃时,固体的成分是________。
②400℃时,样品继续分解得到一种混合气体,该混合气体能使澄清的石灰水变浑浊,也能使灼热的CuO出现红色,则400℃时样品发生反应的化学方程式为________。
③取350℃时的上述样品![]() 难溶于水
难溶于水![]() ,置入0.12mol/L、
,置入0.12mol/L、![]() 的酸性
的酸性![]() 溶液中,二者恰好反应,写出该反应的离子方程式________。
溶液中,二者恰好反应,写出该反应的离子方程式________。
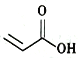
【题目】A、B、M、N四种有机物的有关信息如下表所示:
A | B | M | N |
比例模型为; | 球棍模型为: | 键线式结构为: | ①能与钠反应,但不能与NaOH溶液反应;②能与M反应生成相对分子质量为100的酯 |
请回答:
(1)A在一定条件下可合成包装塑料,反应的化学方程式为____________。
(2)在Ni作催化剂的条件下,B与氢气加热时反应的化学方程式为______________。
(3)M的分子式为__________,M与N反应的化学方程式为_______________。
(4)满足下列条件的M的同分异构体的结构简式为______________。
I:链状 ii:只含一种官能团 iii:能与新制氢氧化铜在加热条件下生成砖红色沉淀