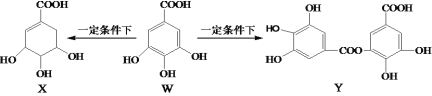��Ŀ����
����Ŀ����������������SO2β�������϶ࣺ
(1)��ԭ��
��Ӧԭ�������º���ʱ2C(s)��2SO2(g)S2(g)��2CO2(g)��һ���¶��£���Ӧ���е���ͬʱ�̲�ø����ʵ�Ũ�Ȳ���ͼ����ͼ��
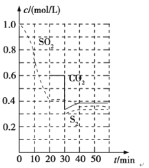
��0��20 min�ڷ�Ӧ���ʱ�ʾΪv(SO2)��________��
��30 minʱ���ı�ijһ����ƽ�ⷢ���ƶ�����ı���������п�����________��
�۸÷�Ӧ��ƽ�ⳣ��K��________��
(2)ѭ�����÷�
��ط�ӦΪ��Na2SO3��SO2��H2O=2NaHSO3����2NaHSO3![]() Na2SO3��SO2����H2O������˵����ȷ����________��
Na2SO3��SO2����H2O������˵����ȷ����________��
A.��Ӧ�ٽ���ʱ����Һ��c(SO32-)/c(HSO![]() )��С����Ӧ�ڽ���ʱ����Һ��c(SO32-)/c(HSO3-)����
)��С����Ӧ�ڽ���ʱ����Һ��c(SO32-)/c(HSO3-)����
B.��Ӧ���뷴Ӧ��Kw��Ϊ10��14
C.ѭ�����õ�������Na2SO3��Һ��β���е�������ѭ�����õĴ�����Ӱ��
D.��Ӧ�ٽ���ʱ��2c(SO32-)��c(HSO3-)��c(OH��)֮�Ͳ���
(3)��ⷨ
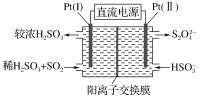
����ͼ��ʾ��Pt(��)�缫�ķ�ӦʽΪ________________��
�ڵ���·��ת��0.02 mol e��ʱ(��ŨH2SO4��δ�ų�)������Ĥ�����Һ��Լ����________ mol���ӡ�
���𰸡�0.03 mol/(L��min) ��СCO2��Ũ�� 0.675 AC SO2��2e����2H2O=SO42-��4H�� 0.03
��������
��1������ͼ��֪��0��20min�ڶ�������Ũ�ȱ仯��Ϊ0.6mol/L������![]() ���㷴Ӧ���ʣ�
���㷴Ӧ���ʣ�
��30 minʱ��������̼��Ũ�Ƚ��ͣ�S2��Ũ�Ȳ��䣬���������̼��S2��Ũ�Ⱦ�����Ӧ���Ǽ�С������̼��Ũ�ȵ��µģ�
�ۻ�ѧƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ������ʹ�Һ���Ũ����Ϊ���������������ʽ��20minʱ����Ӧ�ﵽƽ��״̬����ʱc(SO2)=0.4mol/L��c(CO2)=0.6mol/L��c(S2)=0.3mol/L���ݴ˼���÷�Ӧ��ƽ�ⳣ����
��2��A.  ����Ӧ�ٽ���ʱ����Һ�������Ӧ�ڽ���ʱ����Һ��ȼ�С��
����Ӧ�ٽ���ʱ����Һ�������Ӧ�ڽ���ʱ����Һ��ȼ�С��
B. Kwֻ���¶��йأ�����Kw����
C. ѭ�����õ�������Na2SO3��Һ��Na2SO3��NaHSO3���ױ�β���е�����������
D. ���ݵ���غ�2c(SO32-)��c(HSO3-)��c(OH��)��c(Na��)��c(H��)���Լ���Һ��c(H��)�ı仯������
��3���ٸ��ݵ缫�����ʻ��ϼ۵ı仯�ж�Pt(��)Ϊ�����������������������ᣬ�缫��ӦΪSO2��2e����2H2O=SO42-��4H����
�����ݵ缫��Ӧʽ��������SO2��2e����2H2O=SO42-��4H����������2HSO3- +2e- +2H+=S2O42-+2H2O���Լ����ӵ��ƶ��жϽ���Ĥ�����Һ��Լ�������ӵ����ʵ�����
��1������ͼ��֪��0��20min�ڶ�������Ũ�ȱ仯��Ϊ0.6mol/L����![]() ��
��
�ʴ�Ϊ��0.03 mol/(L��min)��
��30 minʱ��������̼��Ũ�Ƚ��ͣ�S2��Ũ�Ȳ��䣬���������̼��S2��Ũ�Ⱦ�����Ӧ���Ǽ�С������̼��Ũ�ȵ��µģ�
�ʴ�Ϊ����СCO2��Ũ�ȣ�
��20min����Ӧ�ﵽƽ��״̬����ʱc(SO2)=0.4mol/L��c(CO2)=0.6mol/L��c(S2)=0.3mol/L����÷�Ӧ��ƽ�ⳣ�� ��
��
�ʴ�Ϊ��0.675��
��2��A.  ����Ӧ�ٽ���ʱ����Һ���������Һ��
����Ӧ�ٽ���ʱ����Һ���������Һ��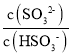 ��С����֮����Ӧ�ڽ���ʱ����Һ��ȼ�С����Һ��
��С����֮����Ӧ�ڽ���ʱ����Һ��ȼ�С����Һ��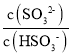 ����A����ȷ��
����A����ȷ��
B. ��Ӧ������ȣ���Kw����10��14��B�����
C. ѭ�����õ�������Na2SO3��Һ��β���е�����������Na2SO3��NaHSO3���Ӷ�Ӱ��������������������ѭ�����õĴ�����C����ȷ��
D. ��Ӧ�ٽ���ʱ��2c(SO32-)��c(HSO3-)��c(OH��)��c(Na��)��c(H��)��c(Na��)���䣬��c(H��)����2c(SO32-)��c(HSO3-)��c(OH��)֮������D�����
�ʴ�Ϊ��AC��
��3������ͼ��֪��Pt(��)�缫�϶����������������ᣬ��õ缫Ϊ�������缫��ӦΪSO2��2e����2H2O=SO42-��4H����
�ʴ�Ϊ��SO2��2e����2H2O=SO42-��4H����
�����ݵ缫��Ӧʽ��������SO2��2e����2H2O=SO42-��4H����������2HSO3- +2e- +2H+
�ʴ�Ϊ��0.03��

����Ŀ�������ϩ����Ҫ���л�����ԭ�ϣ��Ʊ�����ϩ�漰�ķ�Ӧ���£�
��.��۷�Ӧ�� ��H��0
��H��0
��.�⻯��Ӧ�� ��H=-100.5kJ��mol-1
��H=-100.5kJ��mol-1
��.����Ӧ�� ��H=-109.4kJ��mol-1
��H=-109.4kJ��mol-1
��1����Ӧ![]() ��H=__kJ��mol-1��
��H=__kJ��mol-1��
��2����۷�Ӧ���ڸ��������н��С�
��������������ʱ�����������˫�����ϩƽ��ת���ʵ�������__��__��
��ʵ�������г�ͨ��ˮ�����Խ���˫�����ϩ�ķе㡣ij�¶��£�ͨ����ѹΪ70kPa��˫�����ϩ��ˮ�������ﵽƽ�����ѹΪ115kPa��˫�����ϩ��ת����Ϊ90%������ϵ��PH2O=__kPa��
��3���о������ϩ�⻯�Ʊ�����ϩ�ڲ�ͬ�¶��´����Ļ��ԡ��±�����Pd/Al2O3Ϊ��������ͬ��Ӧʱ���ò�ͬ�¶ȵ����ݣ�����������ͬ����
�¶�/�� | 25 | 30 | 35 | 40 | 45 |
�����ϩת����/% | 84.9 | 93.9 | 100.0 | 100.0 | 100.0 |
����ϩѡ����/% | 81.3 | 88.6 | 75.5 | 60.6 | 51.3 |
˵����ѡ����=![]() ��100%������=
��100%������=![]() ��100%��
��100%��
�������������������Ļ��ԡ�
����ѵķ�Ӧ�¶�Ϊ__��ѡ����¶ȵ�ԭ����__��
�ڱ���ʵ�����ݱ����������¶ȣ������ϩת������߶�����ϩѡ���Խ��ͣ���ԭ����__��