题目内容
20.下列各组元素中,按最高正化合价递增顺序排列的是( )| A. | C、N、F | B. | Na、Mg、Al | C. | F、Cl、Br | D. | Cl、S、P |
分析 元素的最高正价=最外层电子数,同主族元素最高正化合价相等,注意氧元素没有最高正价,氟元素无正价,据此分析.
解答 解:A.F元素没有最高正化合价,故A错误;
B.Na、Mg、Al最外层电子数依次为1、2、3,其最高化合价分别为+1、+2,+3,故B正确;
C.F元素没有最高正化合价,Cl、Br位于同一主族,最外层电子数均为7,其最高化合价均为+7,故C错误;
D.Cl、S、P最外层电子数依次为7、6、5,其最高化合价分别为+7、+6,+5,故D错误.
故选B.
点评 本题考查原子结构与性质关系,难度不大,注意主族元素最高正化合价=最外层电子数=主族族序数,但氧、氟元素没有最高正价.

练习册系列答案
相关题目
10.(共4分)铬酸根CrO42-呈黄色,重铬酸根Cr2O72-呈橙色.在水溶液中,铬酸根离子和重铬酸根离子存在下列平衡:Cr2O72-+H2O?2CrO42-+2H+.在两支试管中分别取重铬酸钾溶液进行下列实验,完成下列表格.
| 试管1:滴加3滴浓硫酸 | 试管2:滴加3滴NaOH溶液 | |
| 实验现象 | ||
| 实验结论 |
8.下列有关物质性质的说法错误的是( )
| A. | 热稳定性:HCl>HI | B. | 原子半径:Na>Mg | ||
| C. | 结合质子能力:S2->Cl- | D. | 酸性:H2SO3>H2SO4 |
5.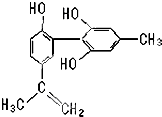 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入KMnO4(H+)溶液,观察紫红色变浅,仅是因为结构中存在碳碳双键 | |
| D. | 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和 H2分别为4mol、7mol |
12.下列物质中最简式相同,但既不是同系物,也不是同分异构体,又不含相同官能团的是( )
| A. | CH3CH=CH2和  | B. | 乙炔和苯 | C. | 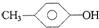 和 和  | D. | 甲醛和甲酸甲酯 |
9.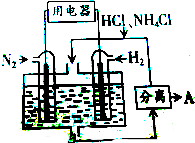 如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
 如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )
如图所示使用新型电极材料 以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池.下列说法正确的是( )| A. | 通氮气的一极为负极 | |
| B. | 通氢气的一极发生还原反应 | |
| C. | 该电池的正极反应式为:N2+6e-+8H+═2NH4+ | |
| D. | 生产中可分离出的物质A的化学式为NH3 |
10.只用一种试剂可区别Na2SO4、MgCl2、Al2(SO4)3、FeCl3四种溶液,这种试剂是( )
| A. | AgNO3 | B. | H2SO4 | C. | BaCl2 | D. | NaOH |