题目内容
11.1mol下列物质在足量氧气中充分燃烧,消耗氧气物质的量最多的是( )| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 乙醇 |
分析 物质的量相同的烃CxHy完全燃烧耗氧量取决于(x+$\frac{y}{4}$),(x+$\frac{y}{4}$)值越大耗氧量越大,据此判断.
解答 解:A、CH4的(x+$\frac{y}{4}$)=2,即1molCH4消耗氧气2mol;
B、C2H4的(x+$\frac{y}{4}$)=2+1=3,即1molC2H4消耗氧气3mol;
C、C6H6的(x+$\frac{y}{4}$)=6+1.5=7.5,即1molC6H6消耗氧气7.5mol;
D、C2H6O(C2H4•H2O)的耗氧相当于C2H4的(x+$\frac{y}{4}$)=2+1=3,即1molC2H6O消耗氧气3mol;
所以相同物质的量耗氧量C6H6>C2H6O=C2H4>CH4.
故选C.
点评 本题考查烃燃烧耗氧量比较,难度不大,关键清楚物质的量相同的烃CxHy完全燃烧耗氧量取决于(x+$\frac{y}{4}$),(x+$\frac{y}{4}$)值越大耗氧量越大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
1.准确移取20.00mL某待测HCl溶液于锥形瓶中,用0.1000mol•L-1NaOH溶液滴定,测HCl溶液得浓度,下列说法正确的是( )
| A. | 滴定前滴定管尖嘴内无气泡,终点读数时有气泡,则测定结果偏小 | |
| B. | 滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定 | |
| C. | 用酚酞作指示剂,当锥形瓶中溶液由粉红色变无色时停止滴定 | |
| D. | 滴定时两眼应注视滴定管中液面的变化 |
2.下列有关叙述中,不正确的是( )
| A. | 硅在元素周期表中的位罝说明硅可用做半导体材料 | |
| B. | 石英可用于制造光导纤维 | |
| C. | 利用铝的金属活泼性可用做铝热剂材料 | |
| D. | 稀硫酸可以钝化铝,所以可以用铝制容器贮运稀硝酸 |
16.下列无色透明的溶液中能大量共存的离子组是( )
| A. | Cu2+、OH-、Al3+、NO3- | B. | H+、CO32-、[Al(OH)4]-、Na+ | ||
| C. | [Al(OH)4]-、OH-、Na+、Cl- | D. | Ba2+、Mg2+、NO3-、SO42- |
20.下列各组顺序的排列正确的是( )
| A. | 原子半径:Br<Cl<F | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO4<H2CO3<H3PO4 | D. | 沸点:乙酸>乙醇>乙烷 |
1.用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 用含0.1molFeCl3的溶液与足量沸水反应制得的Fe(OH)3胶体粒数为0.1NA | |
| B. | 46gNO2和N2O4的混合气体中含N原子总数为NA | |
| C. | 标准状况下,5.6LCCl4含有的分子数为0.25NA | |
| D. | 0.25molNa2O2中含有的阴离子数为0.5NA |
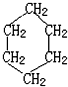 ,名称是环己烷
,名称是环己烷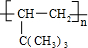 .
. 298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.
298K时,某容积固定为1L的密闭容器中发生如下可逆反应:A(g)?2B(g)△H=akJ•mol-1.其中B的物质的量浓度随时间变化如图所示.试回答下列问题.