题目内容
2.下列有关叙述中,不正确的是( )| A. | 硅在元素周期表中的位罝说明硅可用做半导体材料 | |
| B. | 石英可用于制造光导纤维 | |
| C. | 利用铝的金属活泼性可用做铝热剂材料 | |
| D. | 稀硫酸可以钝化铝,所以可以用铝制容器贮运稀硝酸 |
分析 A、硅处于金属与非金属交界的元素可以作半导体材料;
B、光导纤维的成份是二氧化硅;
C、铝热反应是指铝与高熔点的氧化物发生氧化还原反应;
D、铝在冷的浓硫酸和浓硝酸中发生钝化.
解答 解:A、硅处于金属与非金属交界处,所以硅既有金属性又有非金属性,可用做半导体,故A正确;
B、光导纤维的成份是二氧化硅,所以石英可用于制造光导纤维,故B正确;
C、铝热反应是指铝与高熔点的氧化物发生氧化还原反应,体现铝的活泼性,用做铝热剂材料,故C正确;
D、铝在冷的浓硫酸和浓硝酸中发生钝化,表面形成致密的氧化膜,而不是稀硫酸和稀硝酸,故D错误;
故选D.
点评 本题考查学生元素以及化合物的性质和应用知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
12.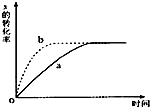 如图曲线a表示放热反应 X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应 X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
 如图曲线a表示放热反应 X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
如图曲线a表示放热反应 X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A. | 升高温度 | B. | 加大X的投入量 | C. | 缩小体积 | D. | 减小N的投入量 |
10.下列表示物质结构的符号或模型不正确的是( )
| A. | N2的结构式:N≡N | B. | CH4分子的比例模型: | ||
| C. | NH3分子的电子式: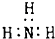 | D. | 乙醇分子的球棍模型: |
17.能正确表示下列反应的离子方程式是( )
| A. | Cl2通入NaOH溶液:Cl2+OH-═Cl-+ClO-+H2O | |
| B. | NaHCO3溶液中加入稀HCl:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| C. | 实验室制取 Cl2:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H20 | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH${\;}_{4}^{+}$ |
7.某有机物的结构式为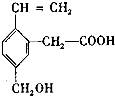 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )
 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )| A. | 能使酸性KMnO4溶液褪色 | B. | 能发生酯化反应 | ||
| C. | 能跟NaOH溶液反应 | D. | 不能发生取代反应 |
14.下列各实验,不可能成功的是( )
①用裂化汽油从碘水中提取碘 ②苯与浓硝酸混合加热至60℃制硝基苯 ③淀粉溶液中加入稀硫酸,煮沸几分钟后,冷却后加入银氨溶液,检验淀粉的水解产物 ④滴加硝酸酸化的硝酸银溶液检验溴乙烷中的溴元素.
①用裂化汽油从碘水中提取碘 ②苯与浓硝酸混合加热至60℃制硝基苯 ③淀粉溶液中加入稀硫酸,煮沸几分钟后,冷却后加入银氨溶液,检验淀粉的水解产物 ④滴加硝酸酸化的硝酸银溶液检验溴乙烷中的溴元素.
| A. | 只有①和④ | B. | 只有②和③ | C. | 只有①和③ | D. | ①②③④ |
11.1mol下列物质在足量氧气中充分燃烧,消耗氧气物质的量最多的是( )
| A. | 甲烷 | B. | 乙烯 | C. | 苯 | D. | 乙醇 |
12.下列有关说法正确的是( )
| A. | 改变物质的性质一定要通过化学变化 | |
| B. | 化学反应必然伴随着能量的变化 | |
| C. | 一种元素可有多种离子,但只有一种原子 | |
| D. | 放热反应一定是不需加热就能发生的 |