题目内容
有Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述中,不正确的是
| A.还原产物为NH4+ |
| B.氧化剂与还原剂的物质的量之比为1∶8 |
| C.若有0.5mol NO3-参加还原反应,则转移电子8mol |
| D.若把该反应设计为电解池,则阳极反应为Fe2+-e→Fe3+ |
C
解析试题分析:Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种微粒属于一个氧化还原反应,Fe3+虽有氧化性,但与H+、NO3-的强氧化性无法比.Fe2+作还原剂,NO3-作氧化剂.由此得出该反应为:8Fe2++NO3-+10H+=8Fe3++NH4++3H2O。A、根据(氧化剂)降(化合价降低) 得(得到电子) 还(发生还原反应),对应产物为还原产物.NO3-生成NH4+,N化合价从+5降为-3,NH4+为还原产物,故A正确;B、根据氧化还原反应的规律:升失氧,降得还;该反应中氧化剂是NO3-,1molNO3-生成1molNH4+,N化合价从+5降为-3,得到8mol电子;还原剂是Fe2+,8molFe2+生成8molFe3+,失去8mol电子,氧化剂与还原剂的物质的量之比为1:8.故B正确;C、氧化剂是NO3-,1molNO3-生成1molNH4+,N化合价从+5降为-3,得到8mol电子,发生还原反应,则0.5mol NO3-参加还原反应,转移电子4mol,故C不正确;D、原电池的负极发生氧化反应,若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+,负极反应是Fe2+失去电子,发生氧化反应.故D正确,答案选C。
考点:考查氧化还原反应的有关判断与计算

利用常温下氨跟氯气能发生置换反应的性质,氯碱工业生产中用来检查氯气是否泄漏,其模拟装置如图。下列有关说法错误的是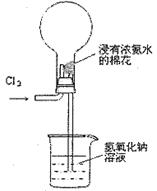
| A.烧瓶中会出现白烟 |
| B.烧瓶中会立即出现喷泉 |
| C.烧瓶中发生的反应表明常温下氨气有还原性 |
| D.烧瓶中还发生化合反应 |
已知反应:Na2O2 + SO2 = Na2SO4,则下列判断正确的是
| A.硫元素被还原 |
| B.二氧化硫是还原剂 |
| C.过氧化钠既是氧化剂又是还原剂 |
| D.二氧化硫既不是氧化剂也不是还原剂 |
将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,共产生NO气体4.48 L(标准状况),向所得溶液中加入物质的量浓度为3 mol·L-1的NaOH溶液至沉淀完全。则下列有关叙述中不正确的是
| A.开始加入合金的物质的量之和为0.3mol |
| B.反应中被还原和未被还原的硝酸物质的量之比为3∶1 |
| C.沉淀完全时消耗NaOH溶液的体积为200mL |
| D.生成沉淀的质量比原合金的质量增加10.2g |
汽车尾气中含有一氧化氮和一氧化碳,消除这两种物质产生的大气污染的方法是安装催化转换器,使它们发生反应生成CO2和N2。反应方程式为:2CO+2NO2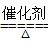 CO2+N2,其中NO2是
CO2+N2,其中NO2是
| A.氧化剂 | B.还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |
常温,下列气体不能共存且发生的反应属于非氧化还原的是
| A.NO和O2 | B.SO2和H2S |
| C.NH3和HCl | D.Cl2和SO2 |
氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
| A.若管道漏气遇氨就会产生白烟 |
| B.该反应利用了Cl2的强氧化性 |
| C.该反应属于复分解反应 |
| D.生成1molN2有6mol电子转移 |
铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:
(1)Tl3++2Ag=Tl++2Ag+
(2)Ag++Fe2+=Ag+Fe3+
(3)Fe+2Fe3+=3Fe2+,
下列离子氧化性比较顺序正确的是
| A.Tl3+>Fe3+>Ag+ | B.Fe3+>Ag+>Tl3+ |
| C.Tl+>Ag+>Fe2+ | D.Tl3+>Ag+>Fe2+ |