��Ŀ����
14��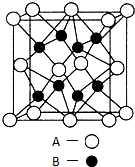 A��B��C��D��E��Ԫ�����ڱ���ԭ���������ε�����ǰ������Ԫ�أ�Aԭ������������Ϊ�ڲ��������3����B����ɫ��Ӧ�ʻ�ɫ��C���⻯����һ��ǿ�ᣬ��Ũ��Һ����A��E�Ļ����ﷴӦ����C�ĵ��ʣ�D��һ�ֽ���Ԫ�أ����̬ԭ������6��δ�ɶԵ��ӣ���ش��������⣺
A��B��C��D��E��Ԫ�����ڱ���ԭ���������ε�����ǰ������Ԫ�أ�Aԭ������������Ϊ�ڲ��������3����B����ɫ��Ӧ�ʻ�ɫ��C���⻯����һ��ǿ�ᣬ��Ũ��Һ����A��E�Ļ����ﷴӦ����C�ĵ��ʣ�D��һ�ֽ���Ԫ�أ����̬ԭ������6��δ�ɶԵ��ӣ���ش��������⣺��1��D�Ļ�̬ԭ�Ӽ۲�����Ų�ʽΪ3d54s1��
��2��C���⻯��ķе������һ����ͬ��Ԫ�ص��⻯��ͣ�����ΪHF���Ӽ�����������HCl���Ӽ������
��3��A��C�縺�Դ�С˳����O��Cl����Ԫ�ط��ű�ʾ����C����ۺ�������Ŀռ乹��Ϊ�������壬������ԭ�ӵ��ӻ�����Ϊsp3��
��4��A��B�γɵĻ�����ľ�����ͼ��ʾ���þ����Ļ�ѧʽΪNa2O������A���ӵ���λ��Ϊ8���þ�������Ϊ���Ӿ��壮
��5���þ����ı߳�Ϊa pm��NA��ʾ����٤������������þ������ܶ�Ϊ$\frac{4��62}{��a��1{0}^{-10}��^{3}{N}_{A}}$g/cm3���г���ʽ����
���� A��B��C��D��E��Ԫ�����ڱ���ԭ���������ε�����ǰ������Ԫ�أ�Aԭ������������Ϊ�ڲ��������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����AΪOԪ�أ�B����ɫ��Ӧ�ʻ�ɫ����BΪNa��C���⻯����һ��ǿ�ᣬ��CΪCl����Ũ��Һ����A��E�Ļ����ﷴӦ����C�ĵ��ʣ�Ӧ�Ƕ���������Ũ���ᷴӦ������������֪EΪMnԪ�أ�D��һ�ֽ���Ԫ�أ����̬ԭ������6��δ�ɶԵ��ӣ����ڵ������ڣ���Χ�����Ų�Ϊ3d54s1����DΪCr���ݴ˽��
��� �⣺A��B��C��D��E��Ԫ�����ڱ���ԭ���������ε�����ǰ������Ԫ�أ�Aԭ������������Ϊ�ڲ��������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����AΪOԪ�أ�B����ɫ��Ӧ�ʻ�ɫ����BΪNa��C���⻯����һ��ǿ�ᣬ��CΪCl����Ũ��Һ����A��E�Ļ����ﷴӦ����C�ĵ��ʣ�Ӧ�Ƕ���������Ũ���ᷴӦ������������֪EΪMnԪ�أ�D��һ�ֽ���Ԫ�أ����̬ԭ������6��δ�ɶԵ��ӣ����ڵ������ڣ���Χ�����Ų�Ϊ3d54s1����DΪCr��
��1��DΪCr�����̬ԭ������6��δ�ɶԵ��ӣ����ڵ������ڣ���̬ԭ�Ӽ۲�����Ų�ʽΪ3d54s1��
�ʴ�Ϊ��3d54s1��
��2��CΪCl������һ����ͬ��Ԫ�ص��⻯��ΪHF��HF���Ӽ�����������HCl���Ӽ����������HCl�ķе����HF��
�ʴ�Ϊ��HF���Ӽ�����������HCl���Ӽ��������
��3��AΪOԪ�ء�CΪClԪ�أ������γɵ���������OԪ�ر��ָ����ϼۣ��Լ��ϵ������������ʵ縺�Դ�С˳����O��Cl��Cl����ۺ������ΪClO4-��Clԭ�Ӽ۲���Ӷ���Ϊ4+$\frac{7+1-2��4}{2}$=4��û�й¶Ե��ӣ�����ռ乹��Ϊ�������壬��Clԭ�ӵ��ӻ�����Ϊsp3�ӻ���
�ʴ�Ϊ��O��Cl���������壻sp3��
��4��������Naԭ����ĿΪ8��Oԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��Na��Oԭ����Ŀ֮��Ϊ8��4=2��1���ʸþ����Ļ�ѧʽΪNa2O��������������A�����о�����֮���ڵ�B������8��������4��λ�����澧���ڲ�����A���ӵ���λ��Ϊ8���þ����������Ӿ��壬
�ʴ�Ϊ��Na2O��8�����Ӿ��壻
��5�������ı߳�Ϊa pm���������Ϊ��a��10-10��3cm3��������Naԭ����ĿΪ8��O������ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4�����Ծ������ܶ�Ϊ$\frac{\frac{23��8+16��4}{{N}_{A}}}{��a��1{0}^{-10}��^{3}}$g/cm3=$\frac{4��62}{��a��1{0}^{-10}��^{3}{N}_{A}}$g/cm3��
�ʴ�Ϊ��$\frac{4��62}{��a��1{0}^{-10}��^{3}{N}_{A}}$��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰�縺�ԡ���������Ų������ṹ���ӻ��������������ȣ�Ҫѧ���þ�̯�����о����ļ��㣬��Ŀ�Ѷ��еȣ�

| A�� | �ý����ƿ������Ҵ������� | |
| B�� | �ø������������Һ�����ּ����3-��ϩ | |
| C�� | ��ˮ�����ֱ����屽 | |
| D�� | ����ˮ�����Ը��������Һ���Լ���1-��ϩ����ȩ |
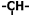 ����������ϩ���ʹμ�֮�����ͨ���Ǽ����������������е����ṹ�Ƿ����е���ϩ�����Ǽ��ĸ�������Ϊ��������
����������ϩ���ʹμ�֮�����ͨ���Ǽ����������������е����ṹ�Ƿ����е���ϩ�����Ǽ��ĸ�������Ϊ��������| A�� | 2����3�� | B�� | 5����3�� | C�� | 4����6�� | D�� | 3����6�� |
| A�� | ��${\;}_{1}^{2}$H��${\;}_{8}^{18}$O����ɵ�11gˮ������������Ϊ6NA | |
| B�� | H2O��D2O����Ϊͬ�������壬�����ߵĻ�ѧ�������� | |
| C�� | ${\;}_{8}^{18}$O2��${\;}_{8}^{16}$O3����Ϊͬλ�� | |
| D�� | ���ʯ��ʯī��Ϊͬ�������壬����֮���ת�����������仯 |
�ٲ��룺
����һ��������Һ��pH��С��
���ض�����Ӧ��ˮԡ�����¶ȣ�
�������ʵ����֤����������һ��������±������ݣ�
�ṩ�Լ�����ȩ��2%ϡ��ˮ��0.25mol/L NaOH��Һ�����ᡢ2% AgNO3��Һ
ʵ����Ʒ���ձ���װ����ˮ�����Թ�
| ʵ�� ���� | ʵ����� | Ԥ�������� ������1ֻд���� |
| 1 | ��A��B��֧�ྻ���Թ��и�����1mL 2%��AgNO3��Һ��Ȼ������Թܱ���ε���2%ϡ��ˮ�� ������ǡ���ܽ⣬��ʱ�Ƶ�pH��ԼΪ8��������Һ�� | �����ɰ�ɫ������������ܽ⣮ |
| 2 | ��A��B�Թܼ���3����ȩ��Ȼ����A�Թ��м�1��NaOH��Һ������֧�Թܷ�����ˮԡ�����ȣ� | ��A�Թܱ�B�Թܳ��ֵ�����ʱ��̡�������������ҺpH��Ӧ���ʿ죻 ��A�Թܱ�B�Թܳ��ֵ�����ʱ�䳤��������ҺpH��Ӧ�������� |
I��ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ��������¶ȶԷ�Ӧ���ʵ�Ӱ�죮�������·������ʵ�飮
| ��Ӧ�� | ���� | �¶� | |
| �� | 10mL10% H2O2��Һ | �� | 25�� |
| �� | 10mL20% H2O2��Һ | �� | 25�� |
| �� | 10mL20% H2O2��Һ | �� | 40�� |
| �� | 10mL20% H2O2��Һ | 1��2��0.1mol/LFeCl3��Һ | 40�� |
��1������ʵ��ٵ�ͼʾ�Ǣ���
��2���Ա�ʵ��ۺܵ͢�Ŀ����̽�������Է�Ӧ���ʵ�Ӱ�죮
��3��ͨ������Ա�ʵ�飬���õ�ʵ������������������䣬����Ӧ��Ũ�Ȼ������¶Ȼ�����������ѧ��Ӧ���ʼӿ죮

��һ���¶��£������Ϊ2L�ĺ����ܱ������г���1molN2��3mol H2��һ�������·�����Ӧ��
N2��g��+3H2��g��?2NH3��g�����������N2���ʵ�����ʱ��仯��ͼ2��ʾ���ش��������⣺
��4���ӿ�ʼ��Ӧ��t2ʱ�̣�������ƽ����Ӧ����Ϊ$\frac{1}{2{t}_{2}}$mol/��L•min����
��5����t3ʱ�̣�������ת����Ϊ75%��
 ����һ����ʹ������ҩ����ɻ�����B��
����һ����ʹ������ҩ����ɻ�����B�� ��ͨ������·�ߺϳɵõ���
��ͨ������·�ߺϳɵõ���
 ��
�� +HBr+CH3Br��
+HBr+CH3Br�� �ȣ�
�ȣ� ��ʾ���ĺϳ�·������ͼ�����Լ���ѡ����
��ʾ���ĺϳ�·������ͼ�����Լ���ѡ����