题目内容
7.观察电子处于1s轨道的电子云图,判断下列说法正确的是( )
| A. | 一个小黑点表示1个自由运动的电子 | |
| B. | 1s轨道的电子云形状为圆形的面 | |
| C. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| D. | 1s轨道电子云图中小黑点的疏密表示电子在某一位置出现机会的多少 |
分析 A.小黑点本身没有意义,不代表1个电子,也不代表出现次数,小黑点的疏密表示出现机会的多少;
B.1s轨道为球形;
C.电子在原子核外作无规则的运动;
D.小黑点的疏密表示出现机会的多少.
解答 解:A.小黑点表示电子在核外空间某处出现的机会,不表示电子数目,故A错误;
B.1s轨道为球形,所以1s轨道的电子云形状为球形,故B错误;
C.电子在原子核外作无规则的运动,不会像地球围绕太阳有规则的旋转,故C错误;
D.小黑点的疏密表示电子在核外单位体积内出现机会的多少,密则机会大,疏则机会小,故D正确;
故选D.
点评 本题考查了1s轨道的电子云等,侧重于基础知识的考查,注意把握电子云的含义,题目难度不大.

练习册系列答案
相关题目
17.(Ⅰ)观察图A、B、C,回答下列问题:
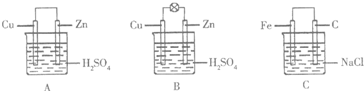
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片没有(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为2H++2e-=H2↑.
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线到铜电极),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol/L、c(ZnSO4)=1mol/L.
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,写出正极的电极反应式O2+2H2O+4e-=4OH-.
(Ⅱ)将铜粉末用10%H2O2和3.0mol•L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是温度升高H2O2的分解速率加快,导致H2O2的浓度降低从而使铜的溶解速率慢.

(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片没有(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为2H++2e-=H2↑.
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线到铜电极),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol/L、c(ZnSO4)=1mol/L.
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,写出正极的电极反应式O2+2H2O+4e-=4OH-.
(Ⅱ)将铜粉末用10%H2O2和3.0mol•L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
2.下列说法正确的是( )
| A. | 具有共价键的化合物就是共价化合物 | |
| B. | 离子化合物不可能全部由非金属构成 | |
| C. | H2O比H2S的沸点高是由于H2O中的O-H键更牢固 | |
| D. | 寻找半导体材料可以在元素周期表的金属与非金属的分界线附近寻找 |
12.下列说法正确的是( )
| A. | π键是由两个p轨道“头碰头”重叠形成的 | |
| B. | σ键一定是有s轨道参与形成的 | |
| C. | 甲烷分子中的键全为σ键而乙烯分子中含σ键和π键 | |
| D. | H2分子中含σ键而Cl2分子中还含π键 |
19.某氧原子的质量为ag,12C原子的质量为bg,且NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 氧元素的相对原子质量为$\frac{12a}{b}$ | B. | 1mol该氧原子质量为aNAg | ||
| C. | xg该氧原子所含的电子数为8xNA | D. | yg该氧原子的中子数一定为$\frac{8y}{a}$ |
16.下列说法正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液的强 | |
| B. | 氨气是弱电解质,铜是强电解质 | |
| C. | 氧化钠是强电解质,醋酸是弱电解质 | |
| D. | 硫酸钠是强电解质,硫酸钡是弱电解质 |
17.下列关于元素周期表中“短周期”的叙述中不正确的是( )
| A. | 共包含18种元素 | B. | 前3周期元素 | ||
| C. | 除稀有气体外,Cl的原子半径最大 | D. | 仅含5种金属元素 |
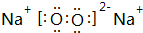 .
.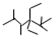 的名称是2,2,4,5-四甲基-3,3-二乙基庚烷,
的名称是2,2,4,5-四甲基-3,3-二乙基庚烷,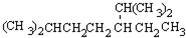 的名称为2,6-二甲基-3-乙基庚烷.
的名称为2,6-二甲基-3-乙基庚烷. ,
,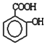 )滴入Na2CO3溶液中发生的化学方程式:
)滴入Na2CO3溶液中发生的化学方程式: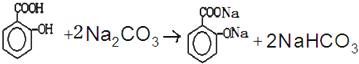 ,
,