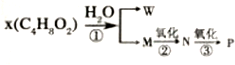题目内容
2.下列说法正确的是( )| A. | 具有共价键的化合物就是共价化合物 | |
| B. | 离子化合物不可能全部由非金属构成 | |
| C. | H2O比H2S的沸点高是由于H2O中的O-H键更牢固 | |
| D. | 寻找半导体材料可以在元素周期表的金属与非金属的分界线附近寻找 |
分析 A.只含共价键的化合物是共价化合物;
B.铵盐是由非金属元素构成的离子化合物;
C.水分子间存在氢键,沸点较高;
D.元素周期表的金属与非金属的分界线处的元素具有金属和非金属的性质.
解答 解:A.具有共价键的化合物可能是离子化合物,如KOH,故A错误;
B.铵盐是离子化合物,铵盐是由非金属元素构成的离子化合物,故B错误;
C.水分子间存在氢键,沸点较高,所以H2O比H2S的沸点高,与共价键强弱无关,故C错误;
D.元素周期表的金属与非金属的分界线处的元素具有金属和非金属的性质,具有半导体性质,故D正确;
故选D.
点评 本题考查了化合物和化学键的关系,明确物质中含有的化学键再结合基本概念来分析解答,会利用举例法分析,题目难度不大.

练习册系列答案
相关题目
12.20℃时,将10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/L的H2SO4溶液混合,3min后溶液中明显出现浑浊.已知温度每升高10℃,化学反应速度增大到原来的3倍,那么40℃时,同样的反应要同样看到浑浊,需要的时间是( )
| A. | 40s | B. | 15s | C. | 30s | D. | 20s |
10.有关图示装置的叙述不正确的是( )
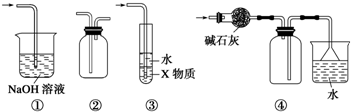

| A. | 装置①可用于吸收实验中多余的SO2 | |
| B. | 装置②可用于收集H2、NH3、Cl2、NO2等 | |
| C. | 装置③中X为苯,可用于吸收氨气或氯化氢 | |
| D. | 装置④可用于收集NH3,并吸收多余的NH3 |
7.观察电子处于1s轨道的电子云图,判断下列说法正确的是( )


| A. | 一个小黑点表示1个自由运动的电子 | |
| B. | 1s轨道的电子云形状为圆形的面 | |
| C. | 电子在1s轨道上运动像地球围绕太阳旋转 | |
| D. | 1s轨道电子云图中小黑点的疏密表示电子在某一位置出现机会的多少 |
14.下列叙述错误的是( )
| A. | 离子键没有方向性和饱和性,而共价键有方向性和饱和性 | |
| B. | 金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 | |
| C. | 配位键在形成时,是由成键双方各提供一个电子形成共用电子 | |
| D. | 三种不同的非金属元素可以形成离子化合物 |
11.下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)金属性最强的元素是钙(填元素名称);
(2)a原子结构示意图为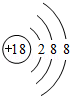 ;
;
(3)与a的电子层结构相同的3种简单离子的半径有小到大的顺序是Ca2+<Cl-<S2-(填离子符号);
(4)g是带来人类文明的重要元素之一,其氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(5)c、d的单质在加热条件下生成物质X,其中含有化学键的类型为离子键、共价键;该物质中阴离子与阳离子个数比1:2.
(6)写出一个由其中某种元素的最高价氧化物对应的水化物与其最低价氢化物反应生成的化合物的化学反应方程式:NH3+HNO3=NH4NO3.
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅤⅡA | O |
| 2 | b | h | c | |||||
| 3 | d | i | g | j | e | a | ||
| 4 | f |
(2)a原子结构示意图为
 ;
;(3)与a的电子层结构相同的3种简单离子的半径有小到大的顺序是Ca2+<Cl-<S2-(填离子符号);
(4)g是带来人类文明的重要元素之一,其氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(5)c、d的单质在加热条件下生成物质X,其中含有化学键的类型为离子键、共价键;该物质中阴离子与阳离子个数比1:2.
(6)写出一个由其中某种元素的最高价氧化物对应的水化物与其最低价氢化物反应生成的化合物的化学反应方程式:NH3+HNO3=NH4NO3.
12.下列实验操作、现象和结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将饱和FeCl3溶液滴入沸水中 | 溶液变红褐色 | 有Fe(OH)3生成 |
| B | 向Na2S溶液中滴加盐酸 | 产生气泡 | Cl的非金属性比S强 |
| C | 向溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中含有SO42- |
| D | 用导线连接铜片和锌片后插进盐酸中 | 铜片上有气泡 | 铜片是原电池的正极 |
| A. | A | B. | B | C. | C | D. | D |

 3-甲基-1-丁烯.
3-甲基-1-丁烯.