题目内容
【题目】Cu2O是一种在涂料、玻璃等领域应用非常广泛的红色氧化物。它不溶于水和醇,溶于盐酸、氯化铵、氨水,易被O2、 硝酸等氧化。一种以硫化铜矿石(含CuFeS2、Cu2S 等) 为原料制取Cu2O 的工艺流程如下:
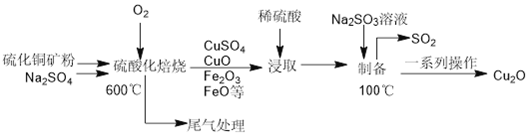
(1) “硫酸化焙烧”时:CuS 与O2反应生成CuSO4等物质的化学方程式为________________;在100℃时,发生反应的离子方程式为________________________________。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是_____________________。
(3) “浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制________________ (至少列举两点)。
(4)得到产品Cu2O的一系列操作主要是___________________________________。
(5)下列有关说法正确的是______________
A.焙烧时得到的尾气可用碱液加以处理
B.Cu2O露置至于空气中会变黑
C.经一系列操作得到产品Cu2O后的副产品,经处理后可作净水剂
D.“制备”时,溶液的pH越小,Cu2O 的产率越高
【答案】 2Cu2S+5O2![]() 2CuSO4+2CuO 2Cu2++3SO32-
2CuSO4+2CuO 2Cu2++3SO32-![]() Cu2O↓+SO42-+2SO2↑ 提高焙烧产物中CuSO4比例 浸取温度、浸取时间、硫酸的浓度等(答出两点即可) 抽滤、洗涤、干燥 ABC
Cu2O↓+SO42-+2SO2↑ 提高焙烧产物中CuSO4比例 浸取温度、浸取时间、硫酸的浓度等(答出两点即可) 抽滤、洗涤、干燥 ABC
【解析】(1)CuS与O2反应生成CuSO4和氧化铜,反应的化学方程式为:2Cu2S+5O2![]() 2CuSO4+2CuO;100℃时,发生反应的离子方程式为2Cu2++3SO32-
2CuSO4+2CuO;100℃时,发生反应的离子方程式为2Cu2++3SO32-![]() Cu2O↓+SO42-+2SO2↑。
Cu2O↓+SO42-+2SO2↑。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是:提高焙烧产物中CuSO4比例。
(3)“浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制浸取温度、浸取时间、硫酸的浓度等。
(4)A.焙烧时得到的尾气为SO2可用碱液加以处理,故A正确;B.Cu2O露置至于空气中会氧化为黑色CuO,故B正确;C.经一系列操作得到产品Cu2O后的副产品硫酸铁,水解产生Fe(OH)3可用作净水剂,故C正确;D.Cu2O在酸溶液中会发生自身氧化还原反应生成Cu和Cu2+,故D错误;本题选ABC。

【题目】常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下:
溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法不正确的是
A. 四种溶液中,Na2CO3溶液中水的电离程度最大
B. NaHSO3溶液显酸性的原因是:电离程度大于水解程度
C. 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
D. 向氯水中加入少量Na2CO3(s),可以增大氯水中次氯酸的浓度


