题目内容
【题目】将4mol A气体和2molB气体置于2L密闭容器中,混合后发生如下反应:2A(g)+B(g)2C(g)+ D(s),若经2s后测得C的浓度为0.6molL-1,下列说法正确的是( )
A. 用物质A表示的反应速率为0.6mol(Ls)-1 B. 2s时物质B的含量为23.3%
C. 2s时物质A的转化率为30% D. 2s时物质B的浓度为0.3molL-1
【答案】C
【解析】起始A的浓度为![]() =2mol/L,B的浓度为
=2mol/L,B的浓度为![]() =1mol/L,经2s后侧得C的浓度为0.6molL-1,
=1mol/L,经2s后侧得C的浓度为0.6molL-1,
2A(g)+B(g)![]() 2C(g),
2C(g),
起始(mol/L) 2 1 0
变化(mol/L)0.6 0.3 0.6
2s时(mol/L)1.4 0.7 0.6
A、2s内,用物质A表示的反应的平均速率为v(A)= ![]() =0.3molL-1s-1,故A错误;B、2s时物质B的含量未注明是物质的量含量还是质量含量,无法计算,故B错误;C、2s时物质A的转化率为α=
=0.3molL-1s-1,故A错误;B、2s时物质B的含量未注明是物质的量含量还是质量含量,无法计算,故B错误;C、2s时物质A的转化率为α=![]() ×100%=30%,故C正确;D、2s时物质B的浓度为1mol/L-0.3mol/L = 0.7molL-1,故D错误;故选C。
×100%=30%,故C正确;D、2s时物质B的浓度为1mol/L-0.3mol/L = 0.7molL-1,故D错误;故选C。

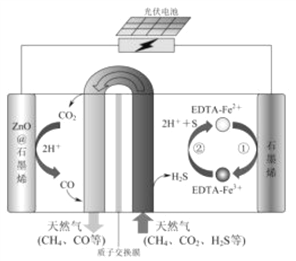
【题目】能源、环境与生产生活和社会发展密切相关。
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收akJ |
①下列情况能说明该反应一定达到平衡状态的是_________(填字母)。
a.v(CO2)消耗=v(CH3OH)生成 b.气体的密度不再随时间改变
c.CO2和CH3OH的浓度之比不再随时间改变 d.气体的平均相对分子质量不再随时间改变
②其他条件不变,达到平衡后,下列不能提高H2转化率的操作是_________(填字母)。
a.降低温度 b.充入更多的H2 c.移除甲醇 d.增大容器体积
③cl_________c2(填“>”、“<”或“=”),a=_________。
④该温度下反应的平衡常数K=_________;若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=_________。
(2)已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是__________(填字母)。
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是__________(填字母)。

A.b点的操作是压缩注射器
B.d点:v正>v逆
C.c点与a点相比,c(NO2)增大,c(N2O4)减小
D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc