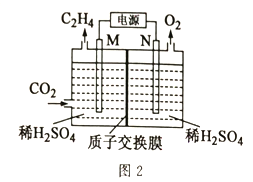
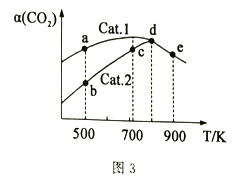
题目内容
【题目】钢材在社会发展中应用广泛。为研究某种碳索钢(含少量碳和硫)的成分,科研小组进行了如下探究活动。
称取碳素钢(已除表面氧化物)24.0g放入耐高温反应管中与O2反应,除去未反应的O2,收集到干燥混合气体X 1.12L(已折算成标准状况下的体积)。
(1)科研小组用下图所示实验装置检验混合气体X的组成。

①装置B中的试剂是___________,装置C的作用是_________。
②若观察到________(填实验现象),证明X中含有CO。
(2)反应后,耐高温反应管内固体中除含有Fe3+之外,还可能含有Fe2+。要确定其中的Fe2+,可选用_______(填序号)。
a.KSCN溶液和氯水 b.KSCN溶液和铁粉
c.稀盐酸和K3[Fe(CN)6]溶液 d.稀H2SO4和KMnO4溶液
(3)科研小组用下图所示装置(部分)测定SO2的体积分数,并计算碳素钢的含碳量。将气体X缓慢通过实验装置,当观察到_____(填实验现象)时,停止通气,此时气体流量仪显示的流量为112mL(已换算成标准状况)。则气体X中SO2的体积分数为_____,碳素钢中碳元素的质量分数为_________(保留1位小数)。

【答案】 品红溶液 验证X中是否含有CO2 E中黑色固体逐渐变红,F中澄清石灰水变浑浊 cd Ⅲ中溶液由蓝色突变为无色 5% 2.4%
【解析】(1)①X中的气体可能是CO、CO2、SO2,酸性高锰酸钾可以除去SO2,B装置装品红溶液检验SO2是否除干净,装置C可以用来检验CO2气体,故答案为:品红溶液;验证X中是否含有CO2。②装置E和F用来检验CO,如果观察到E中黑色固体逐渐变红,F中澄清石灰水变浑浊,说明X中有CO。
(2)首先用酸将耐高温管中的Fe的氧化物转化为离子,K3[Fe(CN)6]溶液遇到亚铁离子会产生蓝色沉淀,KMnO4溶液会将亚铁离子氧化,紫色褪去,故选cd。
(3)该实验是通过二氧化硫与碘单质反应测定二氧化硫的含量,碘遇淀粉变蓝,当Ⅲ中溶液由蓝色突变为无色时说明碘恰好反应完了,测试可以测得消耗二氧化硫的量。发生反应SO2+I2+2H2O=H2SO4+2HI,参与反应的二氧化硫的量为n(SO2)=n(I2)=0.01×0.025=0.00025mol,n(X)=0.112L÷22.4L/mol=0.005mol,二氧化硫体积分数为0.00025÷0.005=0.05,体积分数为5%。混合气体的物质的量为1.12L÷22.4L/mol=0.05mol,X中C原子的物质的量为0.05mol×(1-0.05)=0.0475mol,碳素钢中碳元素的质量分数为(12g/mol×0.0475mol) ÷24g×100%=2.4%,故答案为:Ⅲ中溶液由蓝色突变为无色;5% ;2.4%。

 名师点拨卷系列答案
名师点拨卷系列答案【题目】C、N、O、Na、Mg、Al、S、Cl是常见的八种元素,根据元素及其化合物性质,回答下列问题:
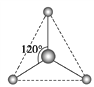
(1)S在周期表中的位置为______;CO2的电子式是_______。
(2)比较O、Na元素常见离子的半径大小(用化学式表示,下同)____>____;__________比较S、Cl元素的最高价氧化物对应水化物的酸性强弱:____>____ 。_______________
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是___________;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
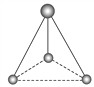
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的结构简式为______;Q的化学式为_______ 。
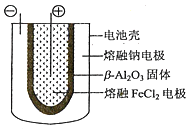
(5)熔融状态下,钠和FeCl2能组成可充电电池(装置示意图如下),反应原理为:2Na+FeCl2![]() Fe+2NaCl.放电时,电池的正极反应式为___________;充电时,_______(写物质名称)电极接电源的负极;该电池的电解质为_______。
Fe+2NaCl.放电时,电池的正极反应式为___________;充电时,_______(写物质名称)电极接电源的负极;该电池的电解质为_______。