题目内容
【题目】下列分子的空间构型可用sp2杂化轨道来解释的是( )
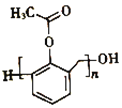
①BF3 ②CH2=CH2 ③![]() ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
A. ①②③ B. ①⑤⑥ C. ②③④ D. ③⑤⑥
【答案】A
【解析】①BF3中B的价层电子对数为3+![]() (3-3
(3-3![]() )=3,中心原子B为sp2杂化,BF3的空间构型为平面三角形;②CH2=CH2中每个C原子形成2个碳氢σ键和1个碳碳双键,双键中有1个σ键和1个π键,C原子上没有孤电子对,C的杂化轨道数为3,C为sp2杂化,CH2=CH2中2个C原子和4个H原子在同一平面上;③
)=3,中心原子B为sp2杂化,BF3的空间构型为平面三角形;②CH2=CH2中每个C原子形成2个碳氢σ键和1个碳碳双键,双键中有1个σ键和1个π键,C原子上没有孤电子对,C的杂化轨道数为3,C为sp2杂化,CH2=CH2中2个C原子和4个H原子在同一平面上;③![]() 中C为sp2杂化,每个C原子形成2个碳碳σ键和1个碳氢σ键,未参与杂化的2p轨道形成一个大π键,
中C为sp2杂化,每个C原子形成2个碳碳σ键和1个碳氢σ键,未参与杂化的2p轨道形成一个大π键,![]() 为平面正六边形结构;④CH
为平面正六边形结构;④CH![]() CH中每个C原子形成1个碳氢σ键和1个碳碳三键,三键中有1个σ键和2个π键,C原子上没有孤电子对,C的杂化轨道数为2,C为sp杂化,CH
CH中每个C原子形成1个碳氢σ键和1个碳碳三键,三键中有1个σ键和2个π键,C原子上没有孤电子对,C的杂化轨道数为2,C为sp杂化,CH![]() CH中2个C原子和2个H原子在同一直线上;⑤NH3中N的价层电子对数为3+
CH中2个C原子和2个H原子在同一直线上;⑤NH3中N的价层电子对数为3+![]() (5-3
(5-3![]() )=4,中心原子N为sp3杂化,NH3的空间构型为三角锥形;⑥CH4中C的价层电子对数为4+
)=4,中心原子N为sp3杂化,NH3的空间构型为三角锥形;⑥CH4中C的价层电子对数为4+![]() (4-4
(4-4![]() )=4,中心原子C为sp3杂化,CH4的空间构型为正四面体形;分子的空间构型可用sp2杂化轨道解释的是①②③,答案选A。
)=4,中心原子C为sp3杂化,CH4的空间构型为正四面体形;分子的空间构型可用sp2杂化轨道解释的是①②③,答案选A。

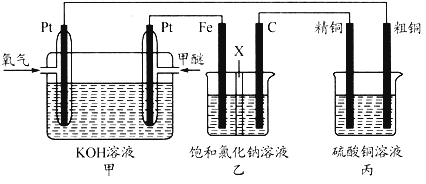
【题目】粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是燃煤发电过程中产生的废渣。粉煤灰的综合利用具有很大的价值。
(1)煤炭在火炉中燃烧很旺时,在往炉膛内的热煤炭上喷洒少量水的瞬间,炉子内火会更旺。如果烧去同量的煤炭,喷洒过水的和没有喷洒过水的煤炭相比较,它们放出的总热量___(填“相同”或“不相同”)。这是因为:________________________。
(2)研究人员通过实验对粉煤灰中铝和铁元素的分离工艺进行了研究。
①以硫酸溶液分解粉煤灰,使其中的铝、铁元素溶出,过滤实现初步分离。向分离所得的滤液中加入还原剂使Fe3+转化为Fe2+,结合下表分析其原因:___________________
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
沉淀区间(pH) | 7.06~895 | 1.94~3.20 | 3.69~4.8 |
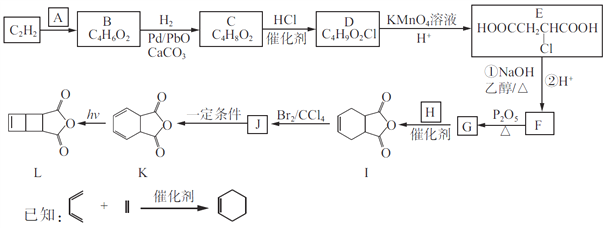
②使用碱性较弱的氨水为pH调节剂,进行分离实验。反应终点的pH对铝和铁分离效果的影响如图1。根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是____________。
(3)工业上可利用煤的气化产物(水煤气)合成甲烷研究得出,甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图2所示。
①T℃时,向1L恒容密闭容器中充入0.3molCH4只发生反应2CH4(g)![]() C2H4(g)+2H2(g)。达到平衡时,测得c(C2H4)=c(CH4)。该反应的△H___(填“>”或“<”)0,CH4的平衡转化率为________。
C2H4(g)+2H2(g)。达到平衡时,测得c(C2H4)=c(CH4)。该反应的△H___(填“>”或“<”)0,CH4的平衡转化率为________。
②列式计算反应2CH4(g)![]() C2H2(g)+3H2(g)在图中A点温度时的平衡常数Kp=________(用平衡分压代替平衡浓度列式计算,不要求写单位,lg0.05=-1.3)。
C2H2(g)+3H2(g)在图中A点温度时的平衡常数Kp=________(用平衡分压代替平衡浓度列式计算,不要求写单位,lg0.05=-1.3)。