��Ŀ����
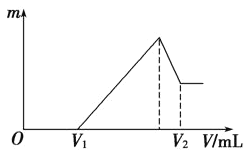
����Ŀ��pC������pH����ָ��ϡ��Һ������Ũ�ȵĸ���������������H2CO3��Һ����εμ�NaOH��Һ�������Һ��pC��pH��ϵ��ͼ��ʾ������˵��������ǣ� ��
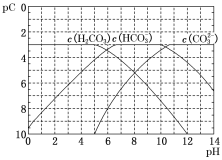
A.��ͬһ��Һ�У�H2CO3��HCO3�C��CO32�C���ܴ�������
B.H2CO3��������ƽ�ⳣ��Ka2������������10�C11
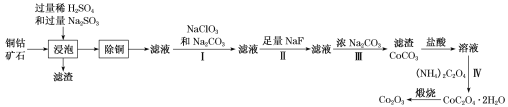
C.��pH=7ʱ����Һ��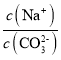 ��3
��3
D.��H2CO3��Һ�μ�NaOH��Һ����Һ�����ԵĹ����У�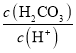 ��С
��С
���𰸡�D
��������
A��H2CO3���������Խ�ǿ����Һ�У�CO32-�����ڼ��Խ�ǿ����Һ�У�������ͬһ��Һ�У�H2CO3��HCO3�C��CO32�C���ܴ������棬A����ȷ��
B�����H2CO3�Ķ�������Ka2=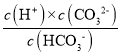 ����ͼ���֪����c(HCO3-)=c(CO32-)��Ka2���ڴ�ʱ��Һ�е�c(H+)����ͼ��֪pH��10��11֮�䣬��H2CO3��������ƽ�ⳣ��Ka2������������10�C11��B����ȷ��
����ͼ���֪����c(HCO3-)=c(CO32-)��Ka2���ڴ�ʱ��Һ�е�c(H+)����ͼ��֪pH��10��11֮�䣬��H2CO3��������ƽ�ⳣ��Ka2������������10�C11��B����ȷ��
C����pH=7ʱ�����ݵ���غ�c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)����֪c(Na+)=c(HCO3-)+2c(CO32-)����ͼ���֪����pH=7ʱ����Һ��c(CO32-)��c(HCO3-)������c(Na+)��3c(CO32-)����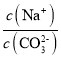 ��3��C����ȷ��
��3��C����ȷ��
D��H2CO3һ������ƽ�ⳣ������ʽKa1=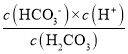 ����H2CO3��Һ�μ�NaOH��Һ����Һ�����ԵĹ����У�c(HCO3-)����Ka1���䣬����
����H2CO3��Һ�μ�NaOH��Һ����Һ�����ԵĹ����У�c(HCO3-)����Ka1���䣬����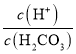 ��С����
������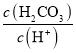 ���D�����
���D�����
��ѡD��

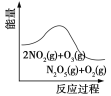
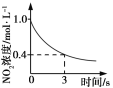
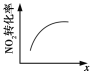
����Ŀ����������������������Լ�����������ӦΪ��2NO2(g)��O3(g) ![]() N2O5(g)��O2(g)������Ӧ�ں����ܱ������н��У������ɸ÷�Ӧ���ͼ���������ж���ȷ����(����)
N2O5(g)��O2(g)������Ӧ�ں����ܱ������н��У������ɸ÷�Ӧ���ͼ���������ж���ȷ����(����)
A | B | C | D |
|
|
|
|
�����¶ȣ�ƽ�ⳣ����С | 0��3 s�ڣ���Ӧ����Ϊ��v(NO2)��0��2 mol��L��1 | t1ʱ�����������ƽ�������ƶ� | ��ƽ��ʱ�����ı�x����xΪc(O2) |
A. AB. BC. CD. D
����Ŀ��ij�о�С����ij2 L�ܱ������м���һ�����Ĺ���A������B��������ӦA(s)��2B(g)![]() D(g)��E(g)����H��Q kJ��mol��1����T��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ��������
D(g)��E(g)����H��Q kJ��mol��1����T��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ��������
������ʱ��(min) ���ʵ���(mol)���������� | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T��ʱ���÷�Ӧ��ƽ�ⳣ��K��________��
(2)30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬���ݱ��е������жϸı������������________(����ĸ���)��
a��ͨ��һ������B b������һ�����Ĺ���A c���ʵ���С��������� d�����߷�Ӧ��ϵ�¶� e��ͬʱ����0.2mol B��0.1mol D��0.1mol E
(3)д�����е������ˮ�еĵ��뷽��ʽ��
CH3COOH��____________NaHSO4��______ NaHCO3��_________H2CO3��_________