题目内容
【题目】CCuS是一种二氧化碳的捕获、利用与封存的技术,这种技术可将CO2资源化, 产生经济效益。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1
反应II:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4kJ·mol-1
2CH3OH(g) △H2=+23.4kJ·mol-1
反应III:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=_____________kJ·mol-1
(2)恒温恒容条件下,在密闭容器中通人等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是_______(填序号)。
A.容器内的混合气体的密度保持不变B.反应体系总压强保持不变
C.CH3OH和CO2的浓度之比保持不变D.断裂3NA个H-O键同时断裂2NA个C=O键
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加人等物质的量的 CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
浓度/mol·L-1 | 1.6 | 1.6 | 0.8 |
此时![]() ___
___![]() (填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH 体积分数 V(CH3OH)%= _____%。
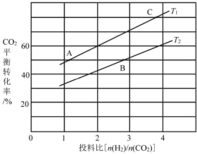
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6 mol CO2和12 mol H2充入3 L的密闭容器中,10 min后反应达到平衡状态,则0-10 min内的平均反应速率V(CH3OCH3)=____。
(5)恒压下将CO2和氏按体积比1 :3混合,在 不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如下图。
其中:CH3OH的选择性=![]() ×100%
×100%
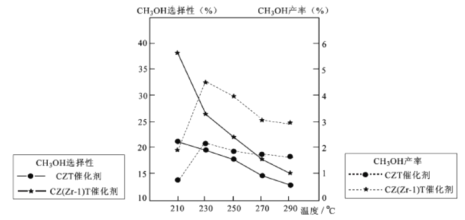
①温度高于230℃,CH3OH产率随温度升高而下降的原因是________。
②在上述条件下合成甲醇的工业条件是_________。
A. 230℃ B. 210℃ C.催化剂 CZT D.催化剂 CZ(Zr-1)T
【答案】-123.0 BCD = 20 ![]() 反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降 AD
反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降 AD
【解析】
(1)根据盖斯定律计算;
(2)达到平衡状态时,v正=v逆,容器内混合气体的平均相对分子质量等于以g/mol为单位的平均摩尔质量,据此分析;
(3)计算浓度商与平衡常数进行比较判断平衡移动方向;体积分数等于物质的量分数;
(4)根据![]() 计算;
计算;
(5)①反应Ⅰ放热,温度升高平衡左移;
②根据图表分析选择合适的温度和催化剂;
(1)由反应I:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1;
CH3OH(g)+H2O(g) △H1=-49.8kJ·mol-1;
反应II:CH3OCH3(g)+H2O(g) ![]() 2CH3OH(g) △H2=+23.4kJ·mol-1
2CH3OH(g) △H2=+23.4kJ·mol-1
可知反应Ⅲ=I×2-II,所以△H3=-49.8kJ·mol-1×2-23.4kJ·mol-1=-123.0 kJ·mol-1;
故答案为:-123.0;
(2)A.容器内的气体体积不变,质量不变,故密度一直不变,故A错误;
B.平衡正向移动时气体体积减小,压强减小,所以压强不变时说明反应达到平衡,故B正确;
C.平衡移动时CH3OH和CO2的浓度变化不一致,所以当比值不变时,说明反应平衡,故C正确;
D.断裂3NA个H-O键,有1molCH3OH和1mol H2O参加反应,同时断裂2NA个C=O键,有1mol CO2参加反应,正反应速率等于逆反应速率,故D正确;
故答案为:BCD。
(3)浓度商Q=![]() =K,故此时达到平衡,
=K,故此时达到平衡,![]() =
=![]() ;体积分数等于物质的量分数,同一容器中可用浓度代替,故V(CH3OH)%=0.8÷(0.8+1.6+1.6)=20%,
;体积分数等于物质的量分数,同一容器中可用浓度代替,故V(CH3OH)%=0.8÷(0.8+1.6+1.6)=20%,
故答案为:=;20
(4)根据图表可知T1温度下投料比为2时,CO2转化率为60%,容器体积为3L,初始浓度c(CO2)=6mol÷3L=2mol/L,c(H2)=12mol÷3L=4 mol/L,CO2转化率为60%,即反应了1.2 mol/L,则生成0.6 mol/L![]() ,反应速率
,反应速率![]() ,
,
故答案为![]() ;
;
(5)①生成甲醇的反应为放热反应,温度升高平衡左移,
故答案为:反应Ⅰ△H<0,温度升高,使CO2转化为甲醇的平衡转化率下降;
②温度不能太低,温度太低反应速率慢,温度也不能过高,过高产率降低,合适温度为230℃;从图表分析催化剂 CZ(Zr-1)T的效果更好,
故答案为AD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列有关说法正确且解释合理的是
说法 | 解释 | |
A | 一定温度压强下,2 g H2 和 4 g H2 完全燃烧,后者 燃烧热的数值大 | 4 g H2 放出热量多 |
B | 2SO2(g)+O2(g) 平衡后再加入 SO2,Q 增大 | 平衡右移,放出热量增多 |
C | 向等物质的量浓度的 NaI 和 KBr 混合液中滴加 AgNO3 溶液,先生成黄色 AgI 沉淀 | Ksp(AgI)<Ksp(AgBr) |
D | 等物质的量浓度 Na2CO3 的 pH 大于 CH3COONa | H2CO3 的酸性比 CH3COOH 强 |
A.AB.BC.CD.D
【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中非金属元素原子的电负性大小顺序是______________。基态K+的电子排布式为__________________。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是_______________,中心原子的杂化方式为__________。NaBH4中存在__________(填标号)。
a.离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为_________________。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:__________________________。
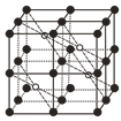
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,若r(F-)=x pm,r(Ca2+)=y pm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=____________________g·cm-3(列出计算表达式)。