��Ŀ����
����Ŀ������˵������ȷ���ǣ� ��
A.ͬһ���淴Ӧʹ�ò�ͬ�Ĵ���ʱ����Ч����������ƽ��ת����
B.��֪��ӦH2O(g) +SO2(g)= H2SO3 (l)���ù�����ֵ����
C.ͬ��ͬѹ�£�H2(g) + Cl2(g) =2HCl(g)�ڹ��պ͵�ȼ�����µ���H��ͬ
D.��֪2H2O(l) =2H2(g) + O2(g) ��H = +571.6 kJ��mol��1��������ȼ����Ϊ285.8 kJ��mol��1
���𰸡�D
��������
Aѡ������ı仯ѧ��Ӧ���ʣ���Ӱ��ƽ���ƶ�����ƽ��ת���ʲ�����ߣ���A����
Bѡ�����Ӧ��2mol��̬���ʷ�Ӧ����1molҺ̬���ʣ���Ϊ��ֵ��С�Ĺ��̣���B����
Cѡ���Ӧ��ȡ���ڷ�Ӧ��ʼ̬����̬���뷴Ӧ���̺������أ������۷�Ӧ�ǵ�ȼ���Ǽ��ȣ���Ӱ�췴Ӧ�ȵ���ֵ����C����
Dѡ�ȼ����ָ1mol��ȼ����ȫȼ�������ȶ��Ļ�����ʱ���ų��������������Ȼ�ѧ����ʽ�ĺ��壬H2�ı�ȼ���ȵ��Ȼ�ѧ����ʽΪ��![]() O2(g) +H2(g) = H2O(l) ��H = ��285.8 kJ��mol��1����D��ȷ��
O2(g) +H2(g) = H2O(l) ��H = ��285.8 kJ��mol��1����D��ȷ��
������������ΪD��

����Ŀ���±���Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����һ��Ԫ�ء�
A | |||||||||||||||||
B | C | D | E | F | T | ||||||||||||
G | H | I | J | K | L | ||||||||||||
M | N | O | |||||||||||||||
�Իش��������⣨ע�⣺ÿ���е���ĸ����Ϊ�ϱ��е���ĸ���ţ�����ΪԪ�ط��ţ�
(1)N�ĵ��ʺ�ˮ������Ӧ�����ɹ���X����I�ĵ�����X��Ӧ�Ļ�ѧ����ʽ_______��
(2)D����̬�⻯���VSEPRģ�͵�����Ϊ_______��
(3)��A��C��D�γɵ�ACD�����У�����������������= _______________��
(4)Ҫ֤��̫�����Ƿ���R Ԫ�أ��ɲ��õķ�����__________________________��
(5)Ԫ��M�Ļ�����(ME2L2)���л��ϳ��п������������Ȼ��������������л��ﷴӦ���ش����⣺
��ME2L2������Ϊ���ɫҺ�壬����CCl4��CS2�Ȼ��ܣ��ݴ˿��ж�ME2L2��_________������ԡ��Ǽ��ԡ������ӡ�
�ڽ�N��O�ĵ����õ������Ӻ����D������������Ӧ��ˮ����Ũ��Һ�У����Ƴ�ԭ��أ�����ɸ������ϵ�Ԫ�ص���Χ���ӹ����ʾʽΪ______________________��
(6)��O2����Һ�м��백ˮ���γ���ɫ�������������백ˮ���������ܽ�����ɫ����Һ��д�������ܽ�����ӷ���ʽ_____��
(7)��F ��K����Ԫ���γɵĻ�����������ԭ�ӵļ۵���ȫ������ɼ�����û�����Ŀռ乹�͵�����Ϊ___��
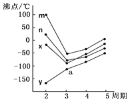
(8)��ͼ�������߷ֱ��ʾ��A�塢��A�塢��A�塢��A��Ԫ����̬�⻯��е�仯����E���⻯�����ڵ�������__����m��n��x��y����
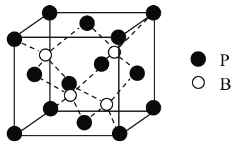
(9)1183 K���´�N����Ļ����ṹ��Ԫ��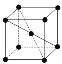 ��ʾ��1183 K����ת��Ϊ
��ʾ��1183 K����ת��Ϊ ��ʾ�ṹ�Ļ����ṹ��Ԫ����1183 K���µľ����У��ռ�������Ϊ____����1183 K���ϵľ����У���Nԭ�ӵȾ����������Nԭ����Ϊ____������ѻ���ʽ������Ϊ_____��
��ʾ�ṹ�Ļ����ṹ��Ԫ����1183 K���µľ����У��ռ�������Ϊ____����1183 K���ϵľ����У���Nԭ�ӵȾ����������Nԭ����Ϊ____������ѻ���ʽ������Ϊ_____��
����Ŀ��CCuS��һ�ֶ�����̼�IJ�����������ļ��������ּ����ɽ�CO2��Դ���� ��������Ч�档CO2��������������ɵ�̼�л����Ҫ�����·�Ӧ��
��ӦI��CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g) ��H1=��49.8kJ��mol��1
CH3OH(g)��H2O(g) ��H1=��49.8kJ��mol��1
��ӦII��CH3OCH3(g)��H2O(g) ![]() 2CH3OH(g) ��H2=��23.4kJ��mol��1
2CH3OH(g) ��H2=��23.4kJ��mol��1
��ӦIII��2CO2(g)��6H2(g) ![]() CH3OCH3(g)��3H2O(g) ��H3
CH3OCH3(g)��3H2O(g) ��H3
��1����H3=_____________kJ��mol��1
��2�����º��������£����ܱ�������ͨ�˵����ʵ�����CO2��H2��������ӦI������������˵����ӦI�ﵽƽ��״̬����_______(����ţ���
A.�����ڵĻ��������ܶȱ��ֲ���B.��Ӧ��ϵ��ѹǿ���ֲ���
C.CH3OH��CO2��Ũ��֮�ȱ��ֲ���D.����3NA��H-O��ͬʱ����2NA��C=O��
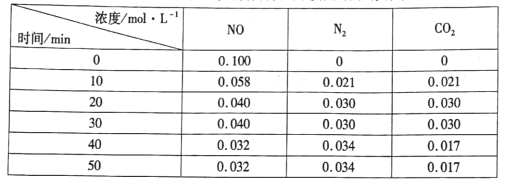
��3����ӦII��ij�¶��µ�ƽ�ⳣ��Ϊ0.25,���¶��£����ܱ������м��˵����ʵ����� CH3OCH3(g)��H2O(g)����Ӧ��ijʱ�̲�ø����Ũ�����£�
���� | CH3OCH3(g) | H2O(g) | CH3OH(g) |
Ũ��/mol��L��1 | 1.6 | 1.6 | 0.8 |
��ʱ![]() ___
___![]() ������>������<������=����������Ӧ�ﵽƽ��״̬ʱ�����������CH3OH ������� V(CH3OH)%= _____%��
������>������<������=����������Ӧ�ﵽƽ��״̬ʱ�����������CH3OH ������� V(CH3OH)%= _____%��
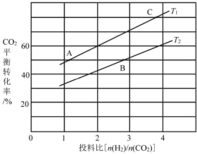
��4����ijѹǿ�£���ӦIII�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ƽ��ת������ͼ��ʾ��T1�¶��£���6 mol CO2��12 mol H2����3 L���ܱ������У�10 min��Ӧ�ﵽƽ��״̬����0-10 min�ڵ�ƽ����Ӧ����V(CH3OCH3)=____��
��5����ѹ�½�CO2���ϰ������1 ��3��ϣ��� ��ͬ���������·�����ӦI�ͷ�ӦIII������ͬ��ʱ�����CH3OH��ѡ���ԺͲ������¶ȵı仯����ͼ��
���У�CH3OH��ѡ����=![]() ��100%
��100%
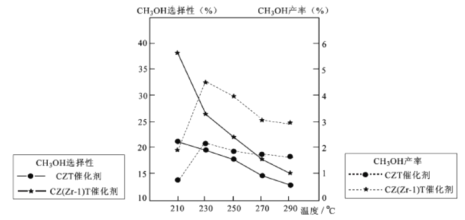
���¶ȸ���230����CH3OH�������¶����߶��½���ԭ����________��
�������������ºϳɼ״��Ĺ�ҵ������_________��
A. 230�� B. 210�� C.���� CZT D.���� CZ(Zr-1)T