题目内容
6.下列离子方程式表达正确的是( )| A. | 少量小苏打溶液和澄清石灰水反应:HCO${\;}_{3}^{-}$+OH-+Ca2+═CaCO3↓+H2O | |
| B. | 氢氧化钡溶液跟硫酸反应:Ba2++SO${\;}_{4}^{2-}$+OH-+H+═BaSO4↑+H2O | |
| C. | 三氯化铁溶液跟氨水反应:Fe3++3OH-═Fe(OH)3↓ | |
| D. | 实验室制二氧化碳:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
分析 A.少量小苏打溶液和澄清石灰水反应,石灰水过量,离子方程式按照碳酸氢钠的化学式书写;
B.氢离子、氢氧根离子的系数不满足硫酸、氢氧化钡的化学式组成;
C.一水合氨为弱碱,一水合氨不能拆开;
D.实验室中用碳酸钙与盐酸制取二氧化碳,碳酸钙不能拆开.
解答 解:A.少量小苏打溶液和澄清石灰水反应生成氢氧化钠、碳酸钙沉淀和水,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故A正确;
B.氢氧化钡溶液跟硫酸反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B错误;
C.三氯化铁溶液跟氨水反应生成氢氧化铁沉淀和氯化铵,正确的离子方程式为:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+,故C错误;
D.实验室用碳酸钙和盐酸反应制二氧化碳,碳酸钙需要保留化学式,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选A.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列说法正确的是( )
①木材纤维和土豆淀粉遇碘水均显蓝色
②食用花生油和鸡蛋清都能发生水解反应
③包装用材料聚乙烯和聚氯乙烯都属于烃
④PX项目的主要产品对二甲苯属于芳香烃
⑤金属钠着火时使用泡沫灭火器灭火
⑥用试管加热碳酸氢钠固体时使试管呈四十五度倾斜
⑦浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
⑧制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片.
①木材纤维和土豆淀粉遇碘水均显蓝色
②食用花生油和鸡蛋清都能发生水解反应
③包装用材料聚乙烯和聚氯乙烯都属于烃
④PX项目的主要产品对二甲苯属于芳香烃
⑤金属钠着火时使用泡沫灭火器灭火
⑥用试管加热碳酸氢钠固体时使试管呈四十五度倾斜
⑦浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
⑧制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片.
| A. | ①④⑥ | B. | ②⑤⑦ | C. | ②④⑧ | D. | ①⑦⑧ |
17.6.02×1022个Fe原子的质量( )
| A. | 56g | B. | 5.6g/mol | C. | 5.6g | D. | 11.2g |
14.下列有关化学实验操作及安全的说法正确的是( )
| A. | 用酒精灯给锥形瓶加热来浓缩溶液 | |
| B. | 实验室不能采用向下排空气法收集CO | |
| C. | 实验室用碳酸钙和稀盐酸反应,气体产物经碱石灰干燥后可得纯净干燥的CO2 | |
| D. | 氢氧化钙溶液存放在配有磨口塞的玻璃瓶中 |
1.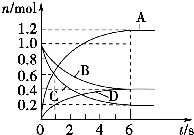 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )| A. | 该反应的化学方程式为3B+4C?6A+2D | |
| B. | 反应进行到1 s时,v(A)和v(D)不相等 | |
| C. | 反应进行到6 s时,B的平均反应速率为0.05 mol•L-1•s-1 | |
| D. | 反应进行到6 s时,各物质的浓度不再变化,反应速率为零 |
11.下列离子方程式正确的是( )
| A. | 硫酸钠溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 大理石与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 氯化铁溶液与碘化钾溶液反应:Fe3++2I-═Fe2++I2 | |
| D. | 氯化镁容液与氨水反应:Mg2++2OH-═Mg(OH)2↓ |
18.下列热化学方程式中△H代表燃烧热的是( )
| A. | CH4 (g)+$\frac{3}{2}$O2(g)═2H2O (l)+CO (g)△H1 | |
| B. | S (s)+$\frac{3}{2}$O2 (g)═SO3 (s)△H2 | |
| C. | C6H12O6 (s)+6O2 (g)═6CO2 (g)+6H2O (l)△H3 | |
| D. | 2CO (g)+O2(g)═2CO2 (g)△H4 |
15.下列说法正确的是( )
| A. | 氨的催化氧化是一种特殊的固氮方式 | |
| B. | Na2O、Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物 | |
| C. | Na2O2晶体中既含有离子键又含有共价键 | |
| D. | 用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |
 如图所示,将一小块钠放在石棉网上加热.回答下列问题:
如图所示,将一小块钠放在石棉网上加热.回答下列问题: