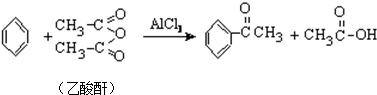
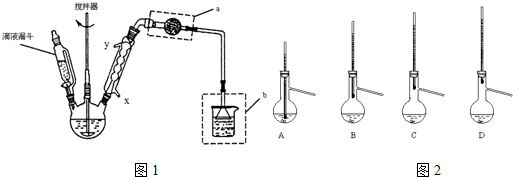
题目内容
17.相同c(H+)的盐酸、醋酸和硫酸均稀释10倍后,c(H+)由大到小的顺序是醋酸>盐酸=硫酸;将体积相同c(H+)相同的盐酸、醋酸和硫酸与足量锌反应,生成氢气的体积(标准状况)大小顺序是醋酸>盐酸=硫酸;
将体积相同浓度相同的盐酸、醋酸和硫酸与足量锌反应,生成氢气的体积(标准状况)大小顺序是硫酸>盐酸=醋酸.
分析 加水稀释促进醋酸的电离,而盐酸和硫酸都是强酸,据此判断稀释后溶液中氢离子浓度大小;
c(H+)相同、体积相同时,生成氢气体积大小与最终氢离子的物质的量成正比;
浓度、体积相同时,溶质的物质的量相同,然后根据三者能够提供氢离子的总物质的量计算出生成氢气的体积之比.
解答 解:相同c(H+)的盐酸、醋酸和硫酸均稀释10倍后,盐酸和硫酸中氢离子浓度都变为原先的$\frac{1}{10}$,而醋酸为弱酸,稀释后醋酸的电离程度增大,醋酸中氢离子浓度大于原先溶液中氢离子浓度的$\frac{1}{10}$,所有稀释后溶液中c(H+)由大到小的顺序是:醋酸>盐酸=硫酸;
将体积相同c(H+)相同的盐酸、醋酸和硫酸与足量锌反应,醋酸为弱酸,醋酸的浓度大于盐酸和硫酸,则醋酸与锌反应生成氢气的体积最大;盐酸和硫酸溶液中氢离子浓度相同,则与锌反应生成氢气的体积相同,所有与锌反应生成氢气体积大小为:醋酸>盐酸=硫酸;
将体积相同浓度相同的盐酸、醋酸和硫酸与足量锌反应,硫酸为二元酸,醋酸和盐酸为一元酸,则与锌反应生成的氢气体积最大,盐酸和醋酸产生的氢气体积相等,则生成氢气的体积(标准状况)大小顺序是:硫酸>盐酸=醋酸,
故答案为:醋酸>盐酸=硫酸;醋酸>盐酸=硫酸;硫酸>盐酸=醋酸.
点评 本题考查了弱电解质的电离平衡及其影响,题目难度中等,明确影响弱电解质的电离平衡的因素为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
5.下列根据实验操作和实验现象所得出的结论不正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向沸水中滴加少量饱和氯化铁溶液,加热至溶液呈红褐色,用激光笔照射 | 有丁达尔效应 | 红褐色液体为胶体 |
| B | 向溶液X中加入NaHCO3粉末 | 产生无色气体 | X一定属于酸 |
| C | 向淀粉NaI溶液中加入氯水 | 溶液变蓝 | 氧化性:Cl2>I2 |
| D | 将气体X分别通入溴水和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是SO2 |
| A. | A | B. | B | C. | C | D. | D |
12.在N2+3H2?2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
| A. | 0.3 mol•L-1•s-1 | B. | 0.4 mol•L-1•s-1 | C. | 0.6 mol•L-1•s-1 | D. | 0.8 mol•L-1•s-1 |
9.用NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 标准状况下,2.24L水所含的分子数目为0.1 NA | |
| B. | 9g水中含有的电子数目为0.5NA | |
| C. | 0.3 mol/L的MgCl2溶液中含Mg2+数目为0.3 NA | |
| D. | 常常压下,28gN2和CO混合气体中所含有的原子数目为2NA |
6.在无色溶液中下列各组离子能大量共存的是( )
| A. | Ag+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Mg2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | Ca2+、Mg2+、Fe2+、Cl- | D. | H+、Na+、CO${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$ |
7.下列关于胶体的叙述不正确的是( )
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在1nm~100nm之间 | |
| B. | 用平行光照射CuSO4溶液和Fe(OH)3胶体,可以加以区分 | |
| C. | 把FeCl3饱和溶液滴入到NaOH溶液中,以制取Fe(OH)3胶体 | |
| D. | 树林中的晨曦,该现象与丁达尔效应有关 |