题目内容
【题目】已知:
①![]()
②![]()
③![]()
则下列叙述正确的是
A.由上述热化学方程式可知![]()
B.甲烷的燃烧热为![]()
C.![]()
![]()
D.若甲醇和甲烷的物质的量之比为![]() ,其完全燃烧生成
,其完全燃烧生成![]() 和
和![]() 时放出的热量为
时放出的热量为![]() ,则该混合物中甲醇的物质的量为
,则该混合物中甲醇的物质的量为![]()
【答案】C
【解析】
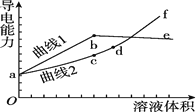
A、气态水到液态水继续放热,所以b<c,故A错误;B、表示燃烧热的热化学方程式中应生成稳定的氧化物,不是水蒸气,应该是液态水,故B错误;C、①![]() ,②
,②![]() ,根据盖斯定律,将2×(①-②)得到:2CH3OH(g)=2CH4(g)+O2(g) △H=2(b-a) kJmol-1,故C正确;D、设:甲醇和甲烷物质的量分别为n、2n,则甲醇放出的热量大于na,甲烷放出的热量是2nc,即na+2nc<Q,解得n<
,根据盖斯定律,将2×(①-②)得到:2CH3OH(g)=2CH4(g)+O2(g) △H=2(b-a) kJmol-1,故C正确;D、设:甲醇和甲烷物质的量分别为n、2n,则甲醇放出的热量大于na,甲烷放出的热量是2nc,即na+2nc<Q,解得n<![]() ,则该混合物中甲醇的物质的量小于
,则该混合物中甲醇的物质的量小于![]() ,与b无关,故D错误;故选C。
,与b无关,故D错误;故选C。

【题目】下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
a | |||||||||||||||||
f | h | i | |||||||||||||||
b | e | j | |||||||||||||||
c | d | g | k | ||||||||||||||
l | |||||||||||||||||
(1)请写出d元素的原子结构示意简图:___________________________________;
(2)请写出i的单质与a、h形成的化合物发生反应的化学方程式_______________________;
(3)请写出上述元素组成的物质间发生的与“(2)”反应类型相同且有固体非金属单质生成的化学反应方程式________________________________________________;
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出g元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式:______________________________________________________;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出j、k的互化物与c、l形成的化合物等物质的量反应时的化学方程式________________。
(6)用电子式表示c、h两种元素以原子个数比1:1形成化合物的形成过程:______________________________________________________。
【题目】一定温度下,在三个容积均为1 L的恒容密闭容器中按不同方式投入反应物,发生反应CO(g)+2H2(g)![]() CH3OH(g)(正反应放热),测得反应的相关数据如下:
CH3OH(g)(正反应放热),测得反应的相关数据如下:
容器 | 容器1 | 容器2 | 容器3 |
反应温度T/K | 500 | 500 | 600 |
反应物投入量 | 1 mol CO、 2 mol H2 | 2 mol CH3OH | 1 mol CO、 2 mol H2 |
平衡v正(H2)/(mol·L-1·s-1) | v1 | v2 | v3 |
平衡c(CH3OH)/(mol·L-1) | c1 | c2 | c3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的转化率α | α1(CO) | α2(CH3OH) | α3(CO) |
平衡常数K | K1 | K2 | K3 |
下列叙述正确的是( )
A. v1<v2,2c1>c2B. α1(CO)>α3(CO),v1<v3
C. p2>2p3,K1<K3D. c2>2c3,α2(CH3OH)+α3(CO)<1
【题目】由![]() 羟基丁酸生成
羟基丁酸生成![]() 丁内酯的反应如下:HOCH2CH2CH2COOH
丁内酯的反应如下:HOCH2CH2CH2COOH![]() +H2O
+H2O
在298K下,![]() 羟基丁酸水溶液的初始浓度为
羟基丁酸水溶液的初始浓度为![]() ,测得
,测得![]() 丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
| 21 | 50 | 80 | 100 | 120 | 160 | 220 |
|
| 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
(1)该反应在50~80min内的平均反应速率为_____![]() 。
。
(2)120min时![]() 羟基丁酸的转化率为______。
羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数![]() _____。
_____。
(4)为提高![]() 羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。