题目内容
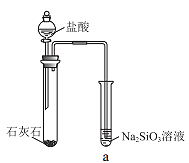
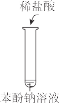
【题目】硅酸(H2SiO3)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用Na2SiO3溶液制备硅酸。某小组同学进行了如下实验:下列结论不正确的是( )
编号 | Ⅰ | Ⅱ |
实验 |
|
|
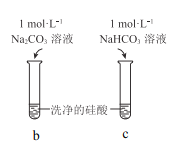
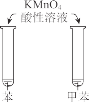
现象 | a 中产生凝胶状沉淀 | b 中凝胶状沉淀溶解,c 中无明显变化 |
A.Na2SiO3溶液一定显碱性
B.由Ⅰ能说明酸性H2CO3>H2SiO3
C.由Ⅱ可知,同浓度时Na2CO3溶液的碱性强于NaHCO3溶液
D.向Na2SiO3溶液中通入少量CO2,发生反应:SiO32-+CO2+H2O=CO32-+H2SiO3↓
【答案】B
【解析】
A.硅酸钠为强碱弱酸盐,SiO32-的水解使得硅酸钠溶液显碱性,故A正确;
B.盐酸与石灰石反应生成二氧化碳,同时挥发出氯化氢,氯化氢也能与硅酸钠反应生成硅酸沉淀,所以由Ⅰ不能说明酸性H2CO3>H2SiO3,故B错误;
C.b 中凝胶状沉淀溶解,c 中无明显变化,说明b碱性更强,即同浓度时 Na2CO3溶液的碱性强于 NaHCO3溶液,故C正确;
D.Na2SiO3溶液中通入少量CO2,反应生成碳酸钠和硅酸,发生反应的离子方程式为:SiO32-+CO2+H2O=CO32-+H2SiO3↓,故D正确;
故答案为B。

 心算口算巧算一课一练系列答案
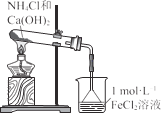
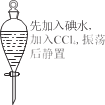
心算口算巧算一课一练系列答案【题目】氯气有毒,且大量制取的难度较大、污染严重,在培养皿中研究氯气的性质可实现“绿色实验”。在培养皿的点滴板中央孔穴中滴加能生成氯气的试剂(如漂白精与盐酸),然后分别滴加所要进行实验的试剂,如图。下列是某学生观察到的现象、解释与结论,其中不符合事实的是
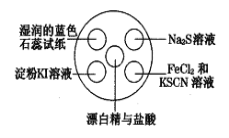
选项 | 实验现象 | 解释 | 结论 |
A | 淀粉KI溶液变蓝 | 氯气置换出KI中的碘使淀粉变蓝 | 单质氧化性:Cl2>I2 |
B | Na2S溶液中出现淡黄色沉淀 | 氯气置换出Na2S中的硫 | 单质氧化性:Cl2>S |
C | 湿润的蓝色石蕊试纸先变红后褪色 | 氯气与水反应生成盐酸和次氯酸 | 氯气具有漂白性 |
D | FeCl2和KSCN溶液的小液滴变红 | FeCl2被Cl2氧化成FeCl3后,再与KSCN溶液反应变红 | 氯气具有氧化性 |
A.AB.BC.CD.D