题目内容
17.将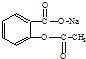 转变为
转变为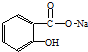 的方法正确的是( )
的方法正确的是( )| A. | 与足量的NaOH溶液共热后,再通入足量的CO2 | |
| B. | 与稀H2SO4共热后,加入足量的Na2CO3 | |
| C. | 与足量的NaOH溶液共热后,加入足量的稀H2SO4 | |
| D. | 与稀H2SO4共热后,加入足量的NaOH |
分析 将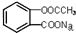 转化为
转化为 先发生水解,再利用强酸制取弱酸的方法实现转化.
先发生水解,再利用强酸制取弱酸的方法实现转化.
解答 解:A.加入足量的NaOH共热后,只有-COOCCH3反应转化为-ONa,再通入足量的CO2,-ONa转化为-OH,故A正确;
B.与稀H2SO4共热后,两个侧链均反应生成-COOH、-OH,加足量的Na2CO3,-OH、-COOH都反应生成-ONa、-COONa,故B错误;
C.加入足量NaOH生成-COONa,再加入足量稀硫酸生成-OH、-COOH,故C错误;
D.与稀H2SO4共热后,两个侧链均反应,加足量的NaOH生成-COONa、-ONa,故D错误;
故选A.
点评 本题考查有机物的合成,侧重有机物官能团的变化及性质的考查,注意强酸制取弱酸的反应原理,题目难度中等.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
7.下列说法正确的是( )
| A. | 分子晶体的熔点比金属晶体的低 | |
| B. | 在晶体中只要有阳离子,一定有阴离子 | |
| C. | 在SiO2晶体中,Si原子与Si-O键数目比为1:2 | |
| D. | 离子化合物中可能含有非极性共价键 |
2.下列离子方程式书写正确的是( )
| A. | NaHSO3溶液中投入过氧化钠粉末:4HSO3-+2Na2O2═4SO32-+O2↑+4Na+ | ||||||||
| B. | AlCl3溶液与烧碱溶液反应,当 n(OH-):n(Al3+ )=7:2时:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | ||||||||
| C. | 钠与CuSO4溶液反应,2Na+Cu2+═Cu↓+2Na+ | ||||||||
| D. | 已知碳酸和次氯酸的电离平衡常数如下:
|
9.把4.48L CO2通过一定量的固体过氧化钠后收集到3.36L气体(标准状况下),则这3.36L气体的质量为( )
| A. | 3.8g | B. | 4.8g | C. | 5.6g | D. | 6.0g |
8.下列事实不能用平衡移动原理解释的是( )
| A. | 蒸馏水和0.1 mol•L-1NaOH溶液中的c(H+),前者大于后者 | |
| B. | 红棕色的NO2加压后颜色先变深后变浅 | |
| C. | 高温及加入催化剂都能使合成氨的反应速率加快 | |
| D. | 用加热蒸干AlCl3溶液的办法不能制得无水AlCl3 |
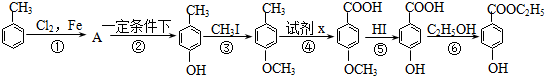
 .
. .
. .
. .
.