题目内容
2.下列离子方程式书写正确的是( )| A. | NaHSO3溶液中投入过氧化钠粉末:4HSO3-+2Na2O2═4SO32-+O2↑+4Na+ | ||||||||
| B. | AlCl3溶液与烧碱溶液反应,当 n(OH-):n(Al3+ )=7:2时:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | ||||||||
| C. | 钠与CuSO4溶液反应,2Na+Cu2+═Cu↓+2Na+ | ||||||||
| D. | 已知碳酸和次氯酸的电离平衡常数如下:
|
分析 A.发生氧化还原反应生成硫酸钠;
B.n(OH-):n(Al3+ )=7:2时,生成等物质的量的氢氧化铝、偏铝酸钠;
C.反应生成氢氧化铜、硫酸钠和氢气;
D.由K可知酸性碳酸>HClO>HCO3-,则碳酸钠与HClO反应.
解答 解:A.NaHSO3溶液中投入过氧化钠粉末的离子反应为2H2O+HSO3-+3Na2O2═SO42-+O2↑+5OH-+6Na+,故A错误;
B.AlCl3溶液与烧碱溶液反应,当 n(OH-):n(Al3+ )=7:2时的离子反应为2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O,故B正确;
C.钠与CuSO4溶液反应的离子反应为2H2O+2Na+Cu2+═Cu(OH)2↓+H2↑+2Na+,故C错误;
D.二氧化碳通入到次氯酸钠溶液中的离子反应为ClO-+CO2+H2O═HCO3-+HClO,故D错误;
故选B.
点评 本题考查离子方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应、强酸制取弱酸的离子反应考查,题目难度不大,选项A为解答的难点.

练习册系列答案
相关题目
12.下列物质是共价化合物的是( )
| A. | KOH | B. | NaCl | C. | H2 | D. | CH4 |
13.短周期元素A、B、C、D在周期表中的位置关系如图所示.已知在同周期元素的常见简单离子中,D的离子半径最小,E是周期表中半径最小的原子
回答下列问题:
(1)C元素在元素周期表中的位置是第二周期第VIA 族.元素D的离子结构示意图为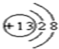
(2)B、E两元素按原子数目比1:3和2:4构成分子X和Y,X的电子式为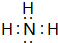 ,Y的结构式为
,Y的结构式为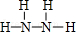 .
.
(3)A、B、C元素的氢化物均有两种或两种以上.在一定条件下A2E4与E2C可发生反应,化学方程式为CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH.
(4)工业上冶炼单质D的化学反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
(5)超细DB粉末被应用于大规模集成电路领域.其制作原理为D2C3、B2、A在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:l;其反应的化学方程式为Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$ 2AlN+3CO.
| A | B | C | |
| D |
(1)C元素在元素周期表中的位置是第二周期第VIA 族.元素D的离子结构示意图为

(2)B、E两元素按原子数目比1:3和2:4构成分子X和Y,X的电子式为
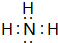 ,Y的结构式为
,Y的结构式为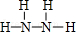 .
.(3)A、B、C元素的氢化物均有两种或两种以上.在一定条件下A2E4与E2C可发生反应,化学方程式为CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH.
(4)工业上冶炼单质D的化学反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
(5)超细DB粉末被应用于大规模集成电路领域.其制作原理为D2C3、B2、A在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:l;其反应的化学方程式为Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$ 2AlN+3CO.
17.将 转变为
转变为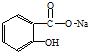 的方法正确的是( )
的方法正确的是( )
 转变为
转变为 的方法正确的是( )
的方法正确的是( )| A. | 与足量的NaOH溶液共热后,再通入足量的CO2 | |
| B. | 与稀H2SO4共热后,加入足量的Na2CO3 | |
| C. | 与足量的NaOH溶液共热后,加入足量的稀H2SO4 | |
| D. | 与稀H2SO4共热后,加入足量的NaOH |
14.有A,B,C,D四个反应:
则在任何温度下都能自发进行的反应是C;在任何温度下都不能自发进行的反应是B;另外两个反应中,在温度高于77℃时可自发进行的反应是A,在温度低于-161.6℃时可自发进行的反应是D.
| 反应 | A | B | C | D |
| △H/(kJ•mol-1) | 10.5 | 1.80 | -126 | -11.7 |
| △S/(J•mol-1•k-1) | 30.0 | -113.0 | 84.0 | -105.0 |
11.在一定条件下,当生成8g SO3气体时,并放出热量9.83kJ.已知SO2在此条件边转化率为80%,据此,下列热化学方程式正确的是( )
| A. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-98.3KJ•mol-1 | |
| B. | 2SO2(g)+O2(g)?2SO3(l);△H=-196.6KJ•mol-1 | |
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-78.64KJ•mol-1 | |
| D. | 2SO2(g)+O2(g)?2SO3(g);△H=+196.6KJ•mol-1 |
13.下列反应中需要加入还原剂才能进行的是( )
| A. | H2→H2O | B. | Zn→Zn2+ | C. | Fe3+→Fe2+ | D. | CuO→CuCl2 |
 ;
;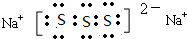 ,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目:
,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目: