题目内容
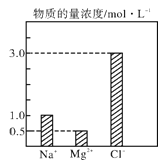
【题目】在0.2 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题
(1)该混合液中,NaCl的物质的量为_________mol,含溶质MgCl2的质量为_______g。
(2)该混合液中CaCl2的物质的量为___________mol,将该混合液加水稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为__________mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
【答案】0.2 9.5 0.1 0.1 0.6
【解析】
由题图可知,n(Na+)=0.2L×1.0mol/L=0.2mol,n(Mg2+)=0.2L×0.5mol/L= 0.1 mol,n(Cl-)=0.2L×3.0mol/L=0.6 mol,据此回答。
由题图可知,n(Na+)=0.2L×1.0mol/L=0.2mol,n(Mg2+)=0.2L×0.5mol/L= 0.1 mol,n(Cl-)=0.2L×3.0mol/L=0.6 mol,
(1)n(NaCl)=0.2 mol,n(MgCl2)=0.1mol,m(MgCl2)=0.1 mol×95 gmol-1=9.5g ;
(2)CaCl2提供的n(Cl-)=0.6mol-0.2 mol-0.1 mol×2=0.2 mol,则n(CaCl2)=0.1 mol,c(CaCl2)=![]() =0.1 molL-1;
=0.1 molL-1;
(3)根据上述推断,溶液中的Cl-的物质的量为0.6mol,根据Cl-+Ag+=AgCl↓,可得到沉淀0.6mol。

练习册系列答案
相关题目