题目内容
8.下列关于Na和Na+性质的叙述正确的是( )| A. | 它们都显碱性 | B. | 它们都有强还原性 | ||
| C. | 它们都能跟H2O、O2反应 | D. | Na只有还原性,Na+只有氧化性 |
分析 A、所谓碱性是OH-的性质,Na+和Na都不显碱性;
B、Na+因最外层有8个电子,反应中不能再失电子;
C、Na+因最外层有8个电子,所以性质很稳定,不与H2O、O2反应;
D、钠单质最外层只有一个电子,易去一个电子,而Na+因最外层有8个电子,只能得电子.
解答 解:A、所谓碱性是OH-的性质,与具体的单质和离子无关,所以Na+和Na都不显碱性,故A错误;
B、Na+因最外层有8个电子,反应中不能再失电子,所以钠离子只具有氧化性,故B错误;
C、Na+因最外层有8个电子,所以性质很稳定,不与H2O、O2反应,故C错误;
D、钠单质最外层只有一个电子,易去一个电子,而Na+因最外层有8个电子,只能得电子,所以Na只有还原性,Na+只有氧化性,故D正确;
故选D.
点评 本题考查钠原子和钠离子的结构和性质,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
18.下列有关化学键与晶体结构的叙述正确的是( )
| A. | 离子晶体在熔化时,离子键被破坏;而分子晶体熔化时,化学键不被破坏 | |
| B. | 12g金刚石中,含C-C共价键键数为4mol | |
| C. | 水晶、干冰熔化时克服粒子间作用力的类型相同 | |
| D. | 熔点由高到低的顺序是:晶体硅>碳化硅>金刚石 |
19.下列物质中,属于高分子化合物的是( )
①蛋白质 ②氨基酸 ③油脂 ④淀粉 ⑤乙烷 ⑥纤维素 ⑦聚乙烯.
①蛋白质 ②氨基酸 ③油脂 ④淀粉 ⑤乙烷 ⑥纤维素 ⑦聚乙烯.
| A. | 只有①⑦ | B. | 除②外都是 | C. | 只有①④⑥⑦ | D. | 只有①③ |
16.下列说法中正确的是( )
| A. | 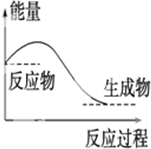 对于如图所示的过程,是放出能量的过程 | |
| B. | 由“C(石墨)=C(金刚石)”反应为吸热,可知,金刚石比石墨稳定 | |
| C. | 由水变成冰是放热反应 | |
| D. | 1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
3.下列各组化合物分子中,键角大小顺序正确的是( )
| A. | BeCl2>BF3>CH4>NH3 | B. | CH4>NH3=BF3>BeCl2 | ||
| C. | BeCl2>BF3=NH3>CH4 | D. | NH3>CH4>BeCl2>BF3 |
13.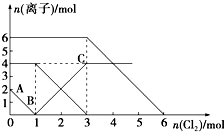 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
 已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 原混合溶液中FeBr2的物质的量为6 mol | |
| C. | 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
20.下列式子是表示氨水中可能存在氢键:①O-H…N ②O-H…O ③N-H…N ④N-H…O.其中正确的是( )
| A. | ①②③④ | B. | ②③④ | C. | ①③ | D. | ②④ |
17.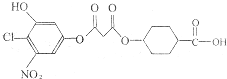 已知苯环上与硝基相邻的卤原子的反应活性很强,易与NaOH溶液发生水解反应.有关如图所示化合物的说法不正确的是( )
已知苯环上与硝基相邻的卤原子的反应活性很强,易与NaOH溶液发生水解反应.有关如图所示化合物的说法不正确的是( )
 已知苯环上与硝基相邻的卤原子的反应活性很强,易与NaOH溶液发生水解反应.有关如图所示化合物的说法不正确的是( )
已知苯环上与硝基相邻的卤原子的反应活性很强,易与NaOH溶液发生水解反应.有关如图所示化合物的说法不正确的是( )| A. | 既可以催化加氢,又可以使酸性高锰酸钾溶液褪色 | |
| B. | 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应 | |
| C. | 1mol该化合物最多可以与7molNaOH反应 | |
| D. | 可以与Br2的CCl4溶液发生加成反应,但不可以在光照下与Br2发生取代反应 |
18.具有以下结构的原子,一定属于主族元素的是( )
| A. | 最外层有3个未成对电子的原子 | B. | 最外层电子排布为ns2的原子 | ||
| C. | 次外层无未成对电子的原子 | D. | 最外层有8个电子的原子 |